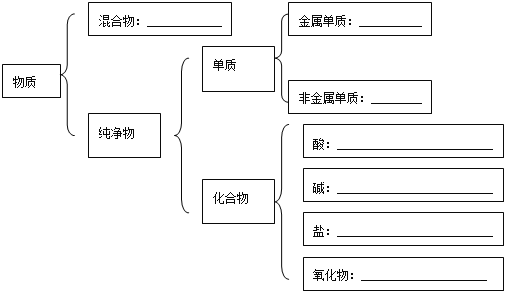
题目内容
【题目】有A、B、C三种可溶性盐,阴、阳离子各不相同,其阴离子的摩尔质量按A、B、C的顺序依次增大。将等物质的量的A、B、C溶于水,所得溶液中只含有Fe3+、K+、SO42-、NO3-、Cl-五种离子,同时生成一种白色沉淀。请回答下列问题:
(1)经检验,三种盐中还含有下列选项中的一种离子,该离子是________。
A. Na+ B. Mg2+ C. Cu2+ D. Ag+
(2)三种盐的化学式分别是A________,B________,C________。
(3)不需要加入任何试剂就能将上述三种盐溶液区分开来,鉴别出来的先后顺序为_______________ (填化学式)。
(4)若将A、B、C三种盐按一定比例溶于水,所得溶液中只含有Fe3+、SO42-、NO3-、K+四种离子且物质的量之比依次为1∶2∶3∶4,则A、B、C三种盐的物质的量之比为____________,若向溶液中加入过量Ba(OH)2,发生反应的总离子方程式为___________________。
【答案】 D FeCl3 AgNO3 K2SO4 FeCl3、AgNO3、K2SO4(或FeCl3、K2SO4、AgNO3) 1∶3∶2 Fe3++2SO![]() +2Ba2++3OH-= 2BaSO4↓+ Fe(OH)3↓
+2Ba2++3OH-= 2BaSO4↓+ Fe(OH)3↓
【解析】等物质的量的A、B、C溶于水,所得溶液中只含有Fe3+、K+、SO42-、NO3-、Cl-五种离子,同时生成一种白色沉淀,A、B、C三种可溶性正盐,阴、阳离子各不相同,其阴离子的摩尔质量依次增大,则A为盐酸盐,B为硝酸盐,C为硫酸盐;等物质的量混合,生成沉淀可能为AgCl,则A为FeCl3,B为AgNO3,C为K2SO4。
(1)由已知,等物质的量的三种物质溶于水,生成一种白色沉淀,已知的三种阴离子与A、B、C三项中的阳离子均不会生成沉淀,故选D。(2)由上述分析可知,A为FeCl3,B为AgNO3,C为K2SO4。(3)观察黄色的溶液为A,与A反应生成白色沉淀的为B,不反应的为C,则检验顺序为A、B、C或(A、C、B),故答案为:FeCl3、AgNO3、K2SO4(或FeCl3、K2SO4、AgNO3)。(4)Fe3+、SO42-、NO3-、K+四种离子且物质的量之比依次为1:2:3:4,则Ag+和Cl-正好反应,设FeCl3为1mol,则AgNO3为3mol,K2SO4为2mol,A、B、C三种正盐的物质的量之比为1:3:2;若向溶液中加入过量Ba(OH)2,则生成BaSO4和Fe(OH)3沉淀,反应的总离子方程式为:Fe3++2SO42- +2Ba2++3OH-= 2BaSO4↓+ Fe(OH)3↓。

【题目】汽车尾气中含有上百种化合物,污染物中以NO为主。请回答下列与NO相关的问题:
(1)汽车发动机工作时燃料燃烧会使氮气转化为NO。
已知:N2(g)+O2(g)=2NO(g) △H=+akJ·mol-1。NO中氮氧键键能为b kJ·mol-1、O=O键能为 c kJ·mol-1。
计算N_N的键能为____________kJ·mol-1(用含a、b、c的代数式表示)。
(2)NO和CO在一定温度和催化剂的条件下可发生反应:
2NO(g)+2CO(g)![]() N2(g)+2CO2(g) △H=-538 kJ·mol-1。
N2(g)+2CO2(g) △H=-538 kJ·mol-1。
一定温度下,向体积为2L的密闭容器中充入一定量的NO和CO,发生上述反应。反应过程中测定的部分数据见下表:
时间/min | n(NO)/mol | n(CO)/mol | n(N2)/mol | n(CO2)/mol |
0 | 0.100 | 0.200 | 0 | 0 |
4 | 0.020 | |||
6 | 0.050 | |||
8 | 0.025 |
①反应在0~4 min内的平均速率v(CO)=_____________。
②下列叙述中,能说明反应已达到平衡的是____________。
a.NO的消耗速率和CO2的生成速率相等 b.容器内的压强不再变化
c.混合气体的密度不再变化 d.N2的百分含量不再变化
③计算该温度下的平衝常数K=____________。
④8min时,其他条件不变,向该反应容器中再通入0.05molNO和0.100CO,重新达到平衡时混合气体中N2的百分含量将____________(填“减小”、“增大”或“不变” )。
(3)工业上采用电解NO的方法制备NH4NO3,其工作原理如图。X、Y皆为Pt电极,为使电解产物全部转化为NH4NO3,需补充NH3。

①Y电极上的电极反应式为_______________________________。
②若X电极上有11.2L(已换算成标准状况)NO发生反应,则生成NH4NO3的质量为____________g。