题目内容
【题目】用电子式表示下列化合物:
(1)NaCl _____。
(2)H2 ______。
(3)MgCl2 ______。
(4)CH4 ______。
(5)CO2 ______。
(6)Na2O ______。
把其中只含共价键的物质的电子式改成结构式: ______、 ______、 ______。
【答案】![]()
![]() :H
:H ![]()
![]()
![]()
![]()
![]()

![]()
【解析】
(1)氯化钠是由钠离子和氯离子形成的离子化合物;
(2)氢气是非金属单质,含有一个氢、氢共价键;
(3)氯化镁是由镁离子和氯离子形成的离子化合物;
(4)甲烷为共价化合物,含有四个碳、氢共价键;
(5)二氧化碳为共价化合物,含有二个碳、氧共价键;
(6)氧化钠是由钠离子和氧离子形成的离子化合物。
(1)氯化钠是由钠离子和氯离子形成的离子化合物,钠离子直接用离子符号表示,氯离子需要标出最外层电子,电子式为![]() ;
;
(2)氢气是非金属单质,含有一个氢、氢共价键,电子式为H:H,结构式为H—H;
(3)氯化镁是由镁离子和氯离子形成的离子化合物,镁离子直接用离子符号表示,氯离子需要标出最外层电子,电子式为![]() ;
;
(4)甲烷为共价化合物,含有四个碳、氢共价键,电子式为![]() ,结构式为
,结构式为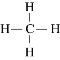 ;
;
(5)二氧化碳为共价化合物,含有二个碳、氧共价键,电子式为![]() ,结构式为O=C=O;
,结构式为O=C=O;
(6)氧化钠是由钠离子和氧离子形成的离子化合物,钠离子直接用离子符号表示,氧离子需要标出最外层电子,电子式为![]() 。
。

【题目】研究CO2的利用对促进低碳社会的构建具有重要的意义。
(1)将CO2与焦炭作用生成CO,CO可用于炼铁等。
已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) ΔH1=+489.0 kJ·mol-1
C(石墨)+CO2(g)=2CO(g) ΔH2=+172.5 kJ·mol-1
则CO还原Fe2O3的热化学方程式为___________________________
(2)某实验将CO2和H2充入一定体积的密闭容器中,在两种不同温度条件下反应:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1
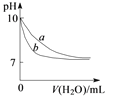
测得CH3OH的物质的量随时间变化如图所示,回答问题:
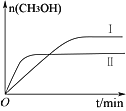
①该反应的平衡常数表达式K=_______________;
②曲线Ⅰ、Ⅱ对应的平衡常数大小关系为:KⅠ_________KⅡ(填“>”、“=”或“<”)。
③下列措施中能增大CO2转化率的是____________。(填序号)
A.升高温度 | B.充入He(g)使体系压强增大 |
C.将H2O(g)从体系中分离 | D.再充入一定量CO2 |
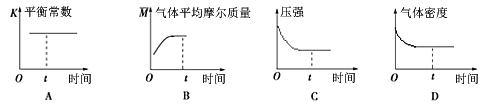
④下列图像正确且能表明在t时刻反应一定处于平衡状态的是__________。(填序号)
【题目】下列实验对应的现象及结论均正确,且两者具有因果关系的是( )
选项 | 实验 | 现象 | 结论 |
A | 室温下,用pH试纸分别测定浓度均为0.1mol·L-1NaClO溶液和CH3COONa溶液的pH | NaClO溶液的pH大于CH3COONa溶液 | HClO的酸性比CH3COOH的酸性弱 |
B | 向盛有2mL0.1mol·L-1AgNO3溶液的试管中滴加5滴0.1mol·L-1Na2CO3溶液,再往试管中滴加几滴0.1mol·L-1Na2S溶液 | 先出现白色沉淀,后沉淀变为黑色 | Ksp(Ag2CO3)>Ksp(Ag2S) |
C | 石灰石与浓盐酸混合共热,将所得气体通入苯酚钠溶液 | 溶液变浑浊 | 碳酸的酸性比苯酚强 |
D | 向2mL0.01mol·L-1的KI溶液中滴入等体积等浓度的FeCl3溶液,将充分反应后的溶液分成三份,第一份滴入K3[Fe(CN)6]溶液,第二份滴入KSCN溶液,第三份滴入淀粉溶液 | 滴入K3[Fe(CN)6]溶液后产生蓝色沉淀;滴入KSCN溶液后溶液变红色;滴入淀粉溶液后溶液变蓝色 | KI溶液和FeCl3溶液发生反应:2Fe3++2I- |
A.AB.BC.CD.D