题目内容
12.甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系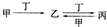 ,下列有关物质的推断正确的是( )
,下列有关物质的推断正确的是( )| A. | 若甲为Al,则丁可能是NaOH溶液 | B. | 若甲为氮气,则丁可能是O2 | ||
| C. | 若甲为Fe,则丁可能是盐酸 | D. | 若甲为Ca(OH)2溶液,则丁可能是CO2 |
分析 A.若甲为Al,丁是NaOH溶液,则乙为偏铝酸钠,偏铝酸钠不与铝反应;
B.若甲为氮气,丁是O2,则乙为NO、丙为NO2,二氧化氮不能与氧气反应得到NO;
C.若甲为Fe,丁是稀盐酸,则乙为氯化亚铁,氯化亚铁与盐酸不反应;
D.若甲为Ca(OH)2溶液,丁是CO2,则乙为CaCO3,丙为Ca(HCO3)2,Ca(HCO3)2与Ca(OH)2反应生成CaCO3;
解答 解:A.若甲为Al,丁是NaOH溶液,则乙为偏铝酸钠,偏铝酸钠不与铝反应,故A错误;
B.若甲为氮气,丁是O2,则乙为NO、丙为NO2,二氧化氮不能与氧气反应得到NO,故B错误;
C.若甲为Fe,丁是稀盐酸,则乙为氯化亚铁,氯化亚铁与盐酸不反应,故C错误;
D.若甲为Ca(OH)2溶液,丁是CO2,则乙为CaCO3,丙为Ca(HCO3)2,Ca(HCO3)2与Ca(OH)2反应生成CaCO3,符合题中各物质转化关系,故D正确,
故选D.
点评 本题考查无机物的推断,综合考查元素化合物性质,关键是掌握物质之间的相互转化,题目难度中等.

练习册系列答案
 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案
相关题目
2.已知1g碳完全燃烧时放出32.79kJ热量,则碳的燃烧热是( )
| A. | 32.79 kJ | B. | 32.79 kJ•mol-1 | C. | 393.5 kJ•mol-1 | D. | 393.5 kJ |
3.用NA表示阿伏加德罗常数,下列说法中正确的是( )
| A. | 在常温常压下,11.2 L氧气所含的原子数目大于NA | |
| B. | 2 L 0.1 mol•L-1 K2SO4溶液中离子总数为1.4 NA | |
| C. | 1 mol H2O2分解制氧气转移电子是2 mol | |
| D. | 16g CH4与18 g NH4+所含电子数相等 |
20.化学与材料、生活和环境密切相关.下列有关说法中错误的是( )
| A. | 绚丽缤纷的烟花中添加了含钾、钙、钠、铜等金属化合物 | |
| B. | 明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 | |
| C. | 光导纤维具有很强的导电能力,故大量用于制造通讯光缆 | |
| D. | 将海水提盐后的苦卤浓缩、氧化,再鼓入热空气可提取中的溴 |
7.进行下列实验,由实验现象得出的结论正确的是( )
| A. | 某气体能使湿润的淀粉KI试纸变蓝,该气体一定是Cl2 | |
| B. | 向某溶液中滴加KSCN溶液,溶液显红色,该溶液中含有Fe3+ | |
| C. | 向某溶液中逐滴滴加稀氨水至过量,先产生白色沉淀然后沉淀溶解,该溶液中含有Al3+ | |
| D. | 向某溶液中通入CO2溶液变浑浊,继续通CO2浑浊消失,该溶液可能是Na2SiO3溶液 |
1.在1.0L密闭容器中放入1.0molX(g),在一定温度进行如下反应:X(g)?Y(g)+Z(g)△H=akJ.mol-1反应时间(t)与容器内气体总压强(p)的数据见下表:
回答下列问题:
(1)实验测得,随温度的升高反应的平衡常数K增大,则△H>0(填>、<或=)
(2)其他条件不变时,为使平衡向右移动,采用的下列措施可行的是BD.
A.缩小容器容积 B.及时分离出Y、Z C.使用合理的催化剂 D.升高体系温度
(3)计算平衡时X的转化率为50%,该温度下反应的平衡常数值为:0.5.
(4)由总压强p和起始压强po表示反应体系的总物质的量n(总)和反应物X的物质的量n(X),则n(总)=$\frac{p}{{p}_{0}}$mol,n(X)=(2-$\frac{p}{{p}_{0}}$)mol,反应物X的转化率a(X)的表达式为($\frac{p}{{p}_{0}}$-1)×100%.
| 时间t/h | 0 | 1 | 2 | 4 | 8 | 16 |
| 总压强p/100kPa | 4.00 | 4.20 | 4.50 | 5.20 | 6.00 | 6.00 |
(1)实验测得,随温度的升高反应的平衡常数K增大,则△H>0(填>、<或=)
(2)其他条件不变时,为使平衡向右移动,采用的下列措施可行的是BD.
A.缩小容器容积 B.及时分离出Y、Z C.使用合理的催化剂 D.升高体系温度
(3)计算平衡时X的转化率为50%,该温度下反应的平衡常数值为:0.5.
(4)由总压强p和起始压强po表示反应体系的总物质的量n(总)和反应物X的物质的量n(X),则n(总)=$\frac{p}{{p}_{0}}$mol,n(X)=(2-$\frac{p}{{p}_{0}}$)mol,反应物X的转化率a(X)的表达式为($\frac{p}{{p}_{0}}$-1)×100%.