题目内容
【题目】下列有机物的同分异构体数目判断错误的是( )
选项 | 有机物 | 同分异构体数目 |
A | 分子式为 | 3 |
B | 分子式为 | 5 |
C | 分子式为 | 4 |
D | 分子式为 | 3 |
A.AB.BC.CD.D
【答案】D
【解析】
根据同分异构体书写规则进行整理,采用“去碳”法依次减少主链碳原子数目进行计算。
A.有机物分子式C5H12为烷烃,同分异构体为正戊烷CH3CH2CH2CH2CH3、异戊烷CH3CH2CH(CH)3、新戊烷C(CH3)4,共有三种结构,A正确;
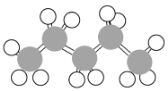
B.含有碳碳双键的有机物分子式为![]() ,即有机物是含有一个碳碳双键的戊烯,同分异构体为1-戊烯CH2=CHCH2CH2CH3、2-戊烯CH3CH=CHCH2CH3(存在顺反异构)、2-甲基-1-丁烯CH2=C(CH3)CH2CH3、2-甲基-2-丁烯CH3C(CH3)═CHCH3、3-甲基-1-戊烯CH3CH(CH3)CH=CH2,共有5种结构(不考虑顺反异构),B正确;
,即有机物是含有一个碳碳双键的戊烯,同分异构体为1-戊烯CH2=CHCH2CH2CH3、2-戊烯CH3CH=CHCH2CH3(存在顺反异构)、2-甲基-1-丁烯CH2=C(CH3)CH2CH3、2-甲基-2-丁烯CH3C(CH3)═CHCH3、3-甲基-1-戊烯CH3CH(CH3)CH=CH2,共有5种结构(不考虑顺反异构),B正确;
C.分子式为![]() ,含有苯环和羟基,即结构可能为含甲基的苯酚或苯甲醇,同分异构体为邻甲基苯酚、对甲基苯酚、间甲基苯酚、苯甲醇,共4种结构,C正确;
,含有苯环和羟基,即结构可能为含甲基的苯酚或苯甲醇,同分异构体为邻甲基苯酚、对甲基苯酚、间甲基苯酚、苯甲醇,共4种结构,C正确;
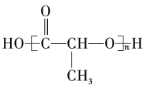
D.分子式为![]() ,含有羧基,即结构可能为正丁酸、2-甲基-丙酸,共2种结构,D错误;
,含有羧基,即结构可能为正丁酸、2-甲基-丙酸,共2种结构,D错误;
答案为D。

【题目】工业上可用隔膜电解槽电解食盐水的方法来制取NaOH、Cl2和H2,并以它们为原料生产一系列化工产品,如次氯酸钠等。根据题意完成下列计算:
(1)某氯碱厂测得某组电解槽的阳极每小时产生气体485.92m3(折算到标准状况,下同),合________________mol;测知其中Cl2的体积分数为0.985(杂质为O2),则该气体的密度为________________;阴极产生NaOH_________mol(保留四位有效数字,下同)。
(2)下表提供了两极溶液浓度的变化数据(阴阳两个极区的物料不流通,忽略其中溶液的体积变化)。
阴极:NaOH溶液质量分数 | 阳极:NaCl溶液浓度(g/L) | |
进料液 | 0.30 | 310 |
电解后 | 0.32 | 210 |
若某个电解槽每小时进NaOH溶液52.000 kg,得到碱溶液初产品90.416 kg,则阳极区每小时加入NaCl溶液_______________m3。取碱溶液初产品中的40% 加入一定量纯水,达到阴极进料液的浓度要求,则需要加入纯水_________________L。
(3)产品之一----漂水(NaClO溶液)具有良好的消毒、漂白能力。在制漂水过程中取1L溶液,测得pH=12(忽略水解),NaClO含量为0.3725g。在一定条件下,将该溶液制成晶体,质量最多为1.335g。通过列式计算,写出该晶体的化学式_________________。