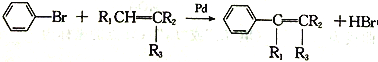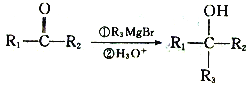题目内容
【题目】如图甲是利用一种微生物将废水中的尿素[CO(NH2)2]的化学能直接转化为电能,并生成环境友好物质的装置,同时利用此装置的电能在铁上镀铜,下列说法中正确的是( )

A. 铜电极应与X相连接
B. H+透过质子交换膜由右向左移动
C. M电极反应式为CO(NH2)2+H2O-6e-===CO2↑+N2↑+6H+
D. 当N电极消耗0.25 mol气体时,则理论上铁电极增重16 g
【答案】C
【解析】A.分析装置甲可知,N电极上由氧气转化为水,氧元素得到电子,发生还原反应,则N电极为原电池的正极;要用乙装置在铁上镀铜,根据电镀原理,铜棒作阳极,铁棒作阴极,所以铜电极要与Y相连,故A错误;装置甲的N极(即正极)反应为O2+4H++4e-=2H2O,M极(即负极)由题干分析可知其电极反应为CO(NH2)2+H2O-6e-=N2↑+CO2↑+6H+,所以H+向N极移动,即由左向右移动,故B错误,C正确;D、当N电极消耗0.25mol气体时,转移n(e-)=0.25mol×4=1mol,根据各电路中电子转移守恒可知,在铁电极上析出铜的质量为m(Cu)= ![]() ×64g/mol=32g,故D错误。本题正确答案为C。
×64g/mol=32g,故D错误。本题正确答案为C。

练习册系列答案
相关题目