题目内容
在一定温度下,固定体积为2L密闭容器中,发生反应:2SO2(g)+O2(g)  2SO3(g) △H<0,n(SO2)随时间的变化如表:
2SO3(g) △H<0,n(SO2)随时间的变化如表:
时间/min | 0 | 1 | 2 | 3 | 4 | 3 |
n(SO2)/mol | 0.20 | 0.1 6 | 0.13 | 0.11 | 0.08 | 0.08 |
则下列说法正确的是
A.当v(SO2)=v(SO3)时,说明该反应已达到平衡状态
B.用O2表示0~4min内该反应的平均速率为0.005mol/(L·min)
C.若升高温度,则SO2的反应速率会变大,平衡常数K值会增大
D.平衡时再通入O2,平衡右移,O2转化率减小,SO2转化率增大
【答案】
D
【解析】
试题分析:以v(SO2)和v(SO3)作为反应达到平衡状态的标志时需说明反应方向;用O2表示0~4min内该反应的平均速率为0.0075mol/(L·min);题中反应放热,升高温度时反应速率变大,但平衡常数K减小。
考点:化学平衡状态、化学平衡常数、物质的转化率。

练习册系列答案
相关题目

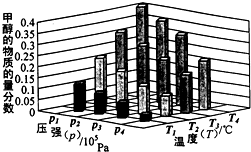 能源是制约国家发展进程的因素之一.甲醇、二甲醚等被称为2 1世纪的绿色能源,工业上利用天然气为主要原料与二氧化碳、水蒸气在一定条件下制备合成气(CO、H2),再制成甲醇、二甲醚.
能源是制约国家发展进程的因素之一.甲醇、二甲醚等被称为2 1世纪的绿色能源,工业上利用天然气为主要原料与二氧化碳、水蒸气在一定条件下制备合成气(CO、H2),再制成甲醇、二甲醚.