题目内容
【题目】还原沉淀法是处理含铬(含Cr2O72-和CrO42-)工业废水的常用方法,过程如下:
![]()
已知转化过程中的反应为2CrO42-(aq)+2H+(aq)![]() Cr2O72-(aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6g/L,CrO42-有10/11转化为Cr2O72-,下列说法不正确的是
Cr2O72-(aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6g/L,CrO42-有10/11转化为Cr2O72-,下列说法不正确的是
A. 溶液颜色保持不变,说明上述可逆反应达到平衡状态
B. 若用绿矾(FeSO4·7H2O)作还原剂,处理1L废水,至少需要458.7g
C. 常温下转化反应的平衡常数K=1×1014,则转化后所得溶液的pH=5
D. 常温下Ksp[Cr(OH)3]=1×10-32,要使处理后废水中的c(Cr3+)降至1×10-5mol/L,应调溶液的pH=5
【答案】C
【解析】试题分析:转化后所得溶液中铬元素含量为28.6g/L,则1L废水中n(Cr)= ![]() =0.55mol。A、存在平衡:2Cr O42-(黄色)+2H+
=0.55mol。A、存在平衡:2Cr O42-(黄色)+2H+![]() Cr2O72-(橙色)+H2O,如颜色不变,说明浓度不变,则达到平衡状态,故A正确;B、若用绿矾(FeSO47H2O)(M=278)作还原剂,处理1L废水,设需要xmolFeSO47H2O,由氧化还原反应中氧化剂和还原剂得失电子数目相等可知0.55×(6-3)=x×(3-2),x=1.65,m(FeSO47H2O)=1.65mol×278g/mol=458.7g,故B正确;C、1L废水中n(Cr)=
Cr2O72-(橙色)+H2O,如颜色不变,说明浓度不变,则达到平衡状态,故A正确;B、若用绿矾(FeSO47H2O)(M=278)作还原剂,处理1L废水,设需要xmolFeSO47H2O,由氧化还原反应中氧化剂和还原剂得失电子数目相等可知0.55×(6-3)=x×(3-2),x=1.65,m(FeSO47H2O)=1.65mol×278g/mol=458.7g,故B正确;C、1L废水中n(Cr)= ![]() =0.55mol,CrO42-有
=0.55mol,CrO42-有![]() 转化为Cr2O72-,则酸化后c(CrO42-)=0.55mol/L×(1-
转化为Cr2O72-,则酸化后c(CrO42-)=0.55mol/L×(1-![]() )=0.05mol/L,c(Cr2O72-)=0.55mol/L×
)=0.05mol/L,c(Cr2O72-)=0.55mol/L×![]() ×
×![]() =0.25mol/L,常温下转换反应的平衡常数K=1×1014,则
=0.25mol/L,常温下转换反应的平衡常数K=1×1014,则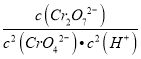 =1×1014,c(H+)=1×10-6mol/L,所以pH=6,故C错误;D、常温下Ksp[Cr(OH)3]=1×10-32,要使处理后废水中c(Cr3+)降至1×10-5mol/L,则c(Cr3+)×c3(OH-)=1×10-32,c(OH-)=1×10-9mol/L,pH=5,故D正确;故选C。
=1×1014,c(H+)=1×10-6mol/L,所以pH=6,故C错误;D、常温下Ksp[Cr(OH)3]=1×10-32,要使处理后废水中c(Cr3+)降至1×10-5mol/L,则c(Cr3+)×c3(OH-)=1×10-32,c(OH-)=1×10-9mol/L,pH=5,故D正确;故选C。

 阅读快车系列答案
阅读快车系列答案