题目内容
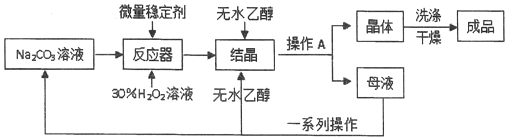
17.紫草宁具有多种生物活性,能抗菌、消炎、抗肿瘤等.合成紫草宁的部分工艺流程如下: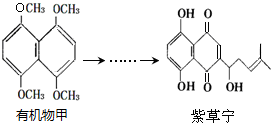
下列说法正确的是( )
| A. | 有机物甲中共有两种化学环境下的氢 | |
| B. | 紫草宁的分子式为C16H18O5 | |
| C. | 紫草宁有8个不饱和度 | |
| D. | 在一定条件下,紫草宁可以发生氧化反应、还原反应、取代反应、加聚反应 |
分析 A、根据对称性原则确定有机物中的等效氢原子数目;
B、根据结构简式书写分子式;
C、1个碳碳双键的不饱和度为1,1个碳环的不饱和度为1,碳碳三键的不饱和度为2,据此结合该有机物的结构简式计算其不饱和度;
D、根据有机物具有的官能团确定有机物的性质.
解答 解:A、根据对称性原则,可以确定有机物中的等效氢原子数目是2,所以有机物甲中共有两种化学环境下的氢,故A正确;
B、根据结构简式,得到有机物的分子式C16H16O5,故B错误;
C、1个碳碳双键的不饱和度为1,1个碳环的不饱和度为1,碳碳三键的不饱和度为2,据此得到该有机物的不饱和度是7,故C错误;
D、有机物具有的官能团:酚羟基、醇羟基和羰基,确定有机物的性质可以发生氧化反应、还原反应、取代反应、加聚反应,故D正确.
故选AD.
点评 本题考查学生有机物的结构和性质知识,注意官能团和有机物的结构和性质之间的关系是关键,难度中等.

练习册系列答案
 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
5.下列关于F、Cl、Br、I的比较,说法不正确的是( )
| A. | 原子最外层的电子数随核电荷数的增加而增多 | |
| B. | 单质颜色随核电荷数的增加而加深 | |
| C. | 氢化物的稳定性随核电荷数的增加而减弱 | |
| D. | 非金属性随核电荷数的增加而减弱 |
2.下列电池工作时,O2在正极放电的是( )
| A. |  甲醇燃料电池 | B. |  镍镉电池 镍镉电池 | C. |  锌锰电池 | D. |  铅蓄电池 铅蓄电池 |
6.下列物质中属于复合材料的是( )
| A. | 水泥 | B. | 玻璃 | C. | 陶瓷 | D. | 玻璃钢 |
7.2.16g X2O5中含有0.1mol氧原子,则X的摩尔质量为( )
| A. | 28 | B. | 28 g•mol-1 | C. | 14 | D. | 14 g•mol-1 |