题目内容
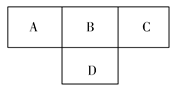
下图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图。下列说法正确的是
| A.该图体现出原子核外电子层呈现周期性变化 |
| B.原子半径:W>R>X |
| C.W的氢化物与R的氢化物水溶液的酸性比较,前者强于后者,可证明非金属性:R>W |
| D.R、Z形成的化合物中可能含有共价键 |
D
解析试题分析:A.该图体现出原子核外电子随原子序数的递增,最外层电子数呈现周期性变化。错误。B.同一周期的元素,原子序数越大,原子半径越小。不同周期的元素,原子核外的电子层数越多,原子半径越大。所以原子半径:R>W>X。错误。C.W、R是同周期的元素。原子序数W>R。原子序数越大,原子半径就越小,元素的非金属性越强。所以非金属性:W > R。错误。D.根据题目提供的信息可知R是S元素,可形成H2S2、H2SO4等多种物质,其中都含有共价键; Z是Na元素,可形成NaOH、Na2O2等多种物质,其中也都含有含有共价键。正确。
考点:考查元素的结构、位置、性质的关系的知识。

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
下列微粒的表示方法能确定为氧离子的是
| A.1S22S22p6 | B.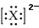 | C.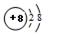 | D.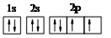 |
俄罗斯科学家在利用回旋加速器进行的实验中,用含20个质子的钙元素的同位素反复轰击含95个质子的镅元素,结果4次成功制成4个第115号元素的原子。这4个原子在生成数微秒后衰变成第113号元素。前者的一种核素为115288X。下列有关叙述正确的是
| A.115号元素衰变成113号元素是化学变化 |
| B.核素115288X的质量数与中子数之差为173 |
| C.113号元素属于非金属元素 |
| D.115号元素的最高正化合价是 +5 |
下列叙述正确的是
| A.非金属元素的原子最外层电子数都大于或等于4 |
| B.只有非金属能形成含氧酸或含氧酸盐 |
| C.非金属元素组成的化合物不一定是共价化合物 |
| D.非金属的最高价含氧酸都具有强氧化性 |
若aAn+与bB2-两种离子的核外电子层结构相同,则a的数值为( )。
| A.b+n+2 | B.b+n-2 | C.b-n-2 | D.b-n+2 |
19世纪中叶,门捷列夫的突出贡献是( )。
| A.提出原子学说 | B.提出分子学说 | C.发现元素周期律 | D.提出电离学说 |
下列各组原子中,彼此的化学性质一定相似的是 ( )
| A.P原子:1s2;Q原子:2s2 |
| B.P原子:M能层上有2个电子;Q原子:N能层上有2个电子 |
| C.P原子:2p能级上有1个未成对电子;Q原子:3p能级上也有1个未成对电子 |
| D.P原子:最外层L能层上只有一个空轨道;Q原子:最外层M能层上也只有一个空轨道 |