��Ŀ����
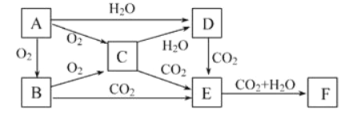
����Ŀ����ͼ�Ƕ����ѽ��ʵ�����̣�����ʾ��������һ���������ѽ�Ŀ��ܷ���ʽΪ��C4H10![]() C2H6+C2H4�� C4H10
C2H6+C2H4�� C4H10![]() CH4+C3H6��
CH4+C3H6��
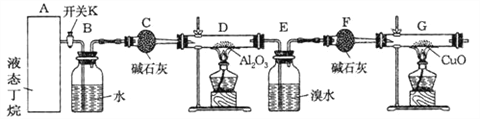
���Ӻ�װ�ú�����е�ʵ������У�
�ٸ�D��Gװ�ü��ȣ��ڼ������װ�õ������ԣ����ų�װ���еĿ�������
��1���������������Ⱥ�˳��������_______________________������ţ�
��2��д������������ͭ��Ӧ�Ļ�ѧ����ʽ______________________
��3������Eװ���еĻ�����ˮ���������ٰ���������ʵ�飺
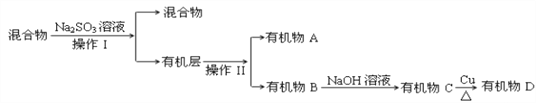
�ٷ�����������������Ʒֱ��ǣ���________��________��Na2SO3��Һ�������ǣ������ӷ���ʽ��ʾ��________________________________________________________��
����֪B��̼ԭ��������A��̼ԭ��������д��B�Ľṹ��ʽ_____________________��
��4���ٶ�������ȫ�ѽ�������E+F��װ�õ��������ȷ�Ӧǰ������0��7 g�� Gװ�õ�����������1��76 g��������ѽ�����м������������ʵ���֮�� n��CH4��: n��C2H6��=__________��
���𰸡� ���� ���� �� CH4+4CuO![]() CO2+2H2O+4Cu ��Һ ����
CO2+2H2O+4Cu ��Һ ���� ![]()
![]() 1��1
1��1
����������K������ͨ��B��Bװ���Ǹ������ݿ����������٣�Cװ�ø��ﶡ�飬�������������������¶��鷢���ѽⷴӦ����ϩ����������E����ˮ����ϩ����F����������G��������Cu�ڼ��������·���������ԭ��Ӧ����Cu��
(1)Ӧ�ȼ��������ԣ��ϳ��ڲ����壬�ٸ�D��Gװ�ü��ȣ��ʴ�Ϊ���ڢۢ���
(2)�����������������������£����������ͭ��Ӧ���ɶ�����̼��ˮ��ͭ����Ӧ����ʽΪ��CH4+4CuO![]() CO2+2H2O+4Cu���ʴ�Ϊ��CH4+4CuO
CO2+2H2O+4Cu���ʴ�Ϊ��CH4+4CuO![]() CO2+2H2O+4Cu��
CO2+2H2O+4Cu��
(3)������к����塢ˮ��������������������ƣ��������Ʊ����������������ƣ�ͬʱ����NaBr���Ӷ���ȥ�壬Ȼ����÷�Һ�������룬���л�����з���õ��л���A���л���B�����л����м���NaOH��Һ���õ��л���C��C�ܷ���������Ӧ����B����ˮ�ⷴӦ����CΪ����C���������õ�ȩD��
��ͨ�����Ϸ���֪�����������͢�����Ʒֱ��ǣ����Һ���������������ƾ��л�ԭ�ԣ��ܺ�ǿ�����������巴Ӧ����ȥ�壬���ӷ���ʽΪ��SO32-+Br2+H2O=SO42-+2Br-+2H+���ʴ�Ϊ����Һ������SO32-+Br2+H2O=SO42-+2Br-+2H+��
����֪B��̼ԭ��������A��̼ԭ������˵��B��̼ԭ�Ӹ�����3��A��̼ԭ�Ӹ�����2��BΪ1��2-������飬B�Ľṹ��ʽCH2BrCHBrCH3���ʴ�Ϊ��CH2BrCHBrCH3��
(4)������ѽ������ɵ���ϩ����������ʵ�����ȣ����ɵļ���ͱ�ϩ�����ʵ�����ȣ�E��F���յ���ϩ����G���ٵ�����������ͭ�е���Ԫ����������xΪC2H4�����ʵ�����yΪC3H6�����ʵ�����������ͼ�������ʵ����ֱ���x��y��28x+42y=0.7g������ͼ��������ͭ��Ӧ��Ҫ����ԭ�ӵ����ʵ���Ϊ2(2x+y)+ ![]() =
=![]() ����ã�x=y=0.07mol���ʴ�Ϊ��1��1��
����ã�x=y=0.07mol���ʴ�Ϊ��1��1��

 ��У���һ��ͨϵ�д�
��У���һ��ͨϵ�д� �γ̴����Ծ�����100��ϵ�д�
�γ̴����Ծ�����100��ϵ�д� �¾�����ĩ���100��ϵ�д�
�¾�����ĩ���100��ϵ�д� ȫ�ܴ���100��ϵ�д�
ȫ�ܴ���100��ϵ�д�����Ŀ������ʵ���ܴﵽԤ��Ŀ�ĵ���
��� | ʵ������ | ʵ��Ŀ�� |
A | ���з�̪��Na2CO3��Һ�м�������BaC12���壬��Һ��ɫ��dz | ֤��Na2CO3��Һ�д���ˮ��ƽ�� |
B | �����£���pH��ֽ�ֱ�ⶨŨ��Ϊ18mol/L��0.1 mol/L H2SO4��Һ��pH | �Ƚϲ�ͬŨ��H2SO4������ǿ�� |
C | ����FeCl2��Һʱ���Ƚ�FeCl2��������Ũ�����У���������ˮϡ�͵�����Ũ�ȣ�������Լ�ƿ�м�������ͭ�� | ����Fe2��ˮ�⣬����ֹFe2�������� |
D | ��ʢ��1mL 0.01 mol/L | ֤������ͬ�¶��µ� Ksp(AgCl)��Ksp(AgI) |
A. A B. B C. C D. D