题目内容
Na2SO3和NaClO两种钠盐分别溶于水后,溶液的pH均大于7,露置于空气中相当一段时间后(不考虑水分挥发)溶液pH都近似为7。这两种溶液呈碱性的原因分别是:_______________________、________________________(用离子方程式表示)。久置呈中性的原因是_____________________________________________________________________。
 +H2O
+H2O
 +OH-,ClO-+H2O====HClO+OH-
+OH-,ClO-+H2O====HClO+OH-Na2SO3水解溶液呈碱性,久置于空气中,Na2SO3被氧化为Na2SO4,溶液呈中性;NaClO水解呈碱性,水解生成的HClO久置于空气中见光分解,NaClO溶液最终变为NaCl溶液,呈?中性。
钠盐溶液pH大于7,一定是钠盐发生了水解,久置于空气中pH近似为7,则是弱酸强碱盐在空气中发生了化学反应转化为强酸强碱盐的缘故。

练习册系列答案
 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
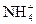 和Cl-四种离子,某同学推测其离子浓度大小顺序有如下四种关系:
和Cl-四种离子,某同学推测其离子浓度大小顺序有如下四种关系: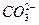
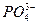
 水解:
水解: NH3·H2O+H+
NH3·H2O+H+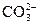 +2H2O
+2H2O H2O+CO2↑+2OH-
H2O+CO2↑+2OH- +H2O
+H2O 、Na+、Cl-、OH-
、Na+、Cl-、OH-
 、Cl-
、Cl- 、K+、
、K+、