题目内容
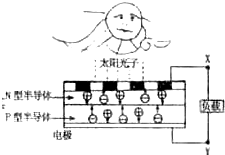
一种氢氧燃料电池用30%KOH溶液为电解质溶液,有关这种电池的说法中错误的是
- A.H2在负极发生氧化反应
- B.供电时的总反应为:2H2 + O2 = 2H2O
- C.产物为无污染的水,属于环境友好电池
- D.负极反应为:H2 - 2e- = 2H+
D
在氢氧燃料电池中,氢气失去电子,发生氧化反应,在负极通入。氧气得到电子,发生还原反应,在正极通入。由于电解质是碱性溶液,所以负极电极反应式为H2-2e-+2OH-=2H2O,即选项D是错误的。答案选D。
在氢氧燃料电池中,氢气失去电子,发生氧化反应,在负极通入。氧气得到电子,发生还原反应,在正极通入。由于电解质是碱性溶液,所以负极电极反应式为H2-2e-+2OH-=2H2O,即选项D是错误的。答案选D。

练习册系列答案
相关题目
 化学在能源开发与利用中起着十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料.
化学在能源开发与利用中起着十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料.