题目内容
【题目】钪及其化合物具有许多优良的性能,在宇航、电子、超导等方面有着广泛的应用。从钛白工业废酸(含钪、钛、铁、锰等离子)中提取氧化钪(Sc2O3)的一种流程如下:

回答下列问题:
(1)洗涤“油相”可除去大量的钛离子。洗涤水是用93%的硫酸、27.5%的双氧水和水按一定比例混合而成。混合的实验操作是____________________________。
(2)先加入氨水调节PH=3,过滤,滤渣主要成分是_____________;再向滤液加入氨水调节pH=6,滤液中 Sc3+ 的浓度为_____________。[25℃时,Ksp[Mn(OH)2]=1.9×10-13、Ksp [Fe(OH)3]=2.6×10-39,Ksp[Sc(OH)3]=9.0×10-31]
(3)用草酸“沉钪”。25℃时pH=2的草酸溶液中 =______________。写出“沉钪”得到草酸钪的离子方程式___________________________________。
=______________。写出“沉钪”得到草酸钪的离子方程式___________________________________。
[25℃时,草酸电离平衡常数为K1=5.0×10-2,K2=5.4×10-5]
(4)草酸钪“灼烧”氧化的化学方程式为_____________________________________。
(5)废酸中含钪量为15mg·L-1, VL废酸最多可提取Sc2O3的质量为_____________。
【答案】 将浓硫酸沿烧杯内壁慢慢注入水中,并用玻璃棒不断搅拌,冷却后再慢慢注入 H2O2中,并不断搅拌。 Fe(OH)3 9.0×10-7mol·L-l 2.7×10-2 2Sc3++ 3H2C2O4=Sc2(C2O4)3↓+ 6H+ 2Sc2(C2O4)3+3O2![]() 2Sc2O3+12CO2 0.023V g
2Sc2O3+12CO2 0.023V g
【解析】(1)洗涤水是用93%的硫酸、27.5%的双氧水和水按一定比例混合而成。混合过程相当于将浓硫酸稀释,因此混合的实验操作为将浓硫酸沿烧杯内壁慢慢注入水中,并用玻璃棒不断搅拌,冷却后再慢慢注入 H2O2中,并不断搅拌,故答案为:将浓硫酸沿烧杯内壁慢慢注入水中,并用玻璃棒不断搅拌,冷却后再慢慢注入 H2O2中,并不断搅拌;
(2)根据Ksp[Mn(OH)2]=1.9×10-13、Ksp [Fe(OH)3]=2.6×10-39,Ksp[Sc(OH)3]=9.0×10-31]可知,溶液的中锰离子完全沉淀时,溶液中的c(OH-)=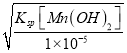 =
=![]() =
=![]() ×10-4=1.37×10-4,溶液的pH约为10,同理铁离子完全沉淀时,溶液中的c(OH-)=
×10-4=1.37×10-4,溶液的pH约为10,同理铁离子完全沉淀时,溶液中的c(OH-)=![]() =
=![]() ×10-11,溶液的pH约为3,钪离子完全沉淀时,溶液中的c(OH-)=
×10-11,溶液的pH约为3,钪离子完全沉淀时,溶液中的c(OH-)=![]() =
=![]() ×10-9,溶液的pH约为5,因此先加入氨水调节PH=3,过滤,滤渣中主要含有Fe(OH)3;再向滤液加入氨水调节pH=6,c(OH-)=10-8=
×10-9,溶液的pH约为5,因此先加入氨水调节PH=3,过滤,滤渣中主要含有Fe(OH)3;再向滤液加入氨水调节pH=6,c(OH-)=10-8= ,解得:c(Sc3+)= 9.0×10-7mol/L,故答案为:Fe(OH)3;9.0×10-7mol/L;
,解得:c(Sc3+)= 9.0×10-7mol/L,故答案为:Fe(OH)3;9.0×10-7mol/L;
(3)根据草酸的电离方程式可知,K1= ,K2=
,K2= ,因此K1K2=
,因此K1K2= ,则
,则 =
= =
= =2.7×10-2,“沉钪”得到草酸钪的离子方程式为2Sc3++ 3H2C2O4=Sc2(C2O4)3↓+ 6H+,故答案为:2.7×10-2;2Sc3++ 3H2C2O4=Sc2(C2O4)3↓+ 6H+;
=2.7×10-2,“沉钪”得到草酸钪的离子方程式为2Sc3++ 3H2C2O4=Sc2(C2O4)3↓+ 6H+,故答案为:2.7×10-2;2Sc3++ 3H2C2O4=Sc2(C2O4)3↓+ 6H+;
(4)草酸钪“灼烧”氧化生成Sc2O3和CO2,反应的化学方程式为2Sc2(C2O4)3+3O2![]() 2Sc2O3+12CO2,故答案为:2Sc2(C2O4)3+3O2
2Sc2O3+12CO2,故答案为:2Sc2(C2O4)3+3O2![]() 2Sc2O3+12CO2;
2Sc2O3+12CO2;
(5)VL废酸中含有钪的质量为15Vmg,根据原子守恒,可提取Sc2O3的质量为15Vmg×![]() =0.023V g,故答案为:0.023V g。
=0.023V g,故答案为:0.023V g。

 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案【题目】探究:1-氯丙烷与NaOH乙醇溶液的反应
学习小组在进行1-氯丙烷与NaOH乙醇溶液溶液的反应中,观察到有气体生成。
请你设计两种不同的方法分别检验该气体。在表中的方框中写出装置中所盛试剂的名称(试剂任选) 和实验现象。
图序 | 装置图 | 所盛试剂 | 实验现象 |
1 |
| A是_________ B是_________ | _________ |
2 |
| C是_______________ | _________ |