题目内容
【题目】使1.0体积的某气态烷烃和烯烃的混合气体在足量空气中完全燃烧,生成2.0体积的二氧化碳和2.2体积的水蒸气(均在120℃、1.01×105Pa条件下测定),则混合气体中烷烃和烯烃的体积比为
A. 2:3 B. 1:4 C. 4:1 D. 3:2
【答案】B
【解析】同温同压下,气体的体积之比等于其物质的量之比,该温度下水为气体,设混合气态烃平均分子组成CxHy,根据质量守恒可得:x=![]() =2、y=
=2、y=![]() =4.4,
=4.4,
则混合烃的平均分子式为:C2H4.4,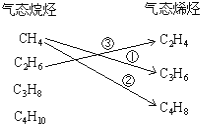
气态烃的碳原子数≤4,则满足C2H4.4合理组合有:①CH4、C3H6②CH4、C4H8③C2H6、C2H4;
①CH4、C3H6:根据平均分子式可知,甲烷与丙烯的物质的量之比为1:1,而平均H原子数为5≠4.4,所以不合理;②CH4、C4H8:平均C原子为2时,设甲烷的物质的量为x、丁烯的物质的量为y,则![]() =2,解得:x:y=2:1,此时得到的混合物中平均H原子数为:
=2,解得:x:y=2:1,此时得到的混合物中平均H原子数为: ![]() =
=![]() ≠4.4,所以不合理;③C2H6、C2H4:二者任意比混合后平均C原子数都是2,氢原子平均数为4.4时,设乙烷的物质的量为x、乙烯的物质的量为y,则:
≠4.4,所以不合理;③C2H6、C2H4:二者任意比混合后平均C原子数都是2,氢原子平均数为4.4时,设乙烷的物质的量为x、乙烯的物质的量为y,则: ![]() =4.4,整理可得:x:y=1:4,满足条件,故选B。
=4.4,整理可得:x:y=1:4,满足条件,故选B。

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目



