题目内容
【题目】用双线桥法表示下列反应的电子转移情况并将其改写成离子方程式: 3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,______________,离子方程式为_________________。
【答案】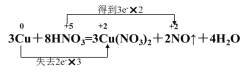 3Cu+8H++2NO3-=3Cu2+ +2NO↑+4H2O
3Cu+8H++2NO3-=3Cu2+ +2NO↑+4H2O
【解析】
氧化还原反应中的,化合价升高值=化合价降低值=转移电子数目,结合双线桥的分析方法解答。
在3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O反应中铜元素由0价变成+2价,硝酸中的氮由+5价变成+2价,所以生成2mol的一氧化氮转移6mol的电子,电子的转移情况用双线桥表示为: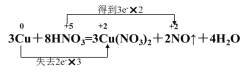 ,反应的离子方程式为3Cu+8H++2NO3-=3Cu2+ +2NO↑+4H2O,故答案为:
,反应的离子方程式为3Cu+8H++2NO3-=3Cu2+ +2NO↑+4H2O,故答案为: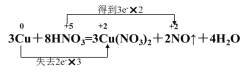 ;3Cu+8H++2NO3-=3Cu2+ +2NO↑+4H2O。
;3Cu+8H++2NO3-=3Cu2+ +2NO↑+4H2O。

练习册系列答案
相关题目