题目内容
【题目】二氧化硫(SO2)是一种在空间地理、环境科学、地质勘探等领域受到广泛研究的一种气体。
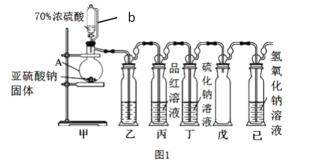
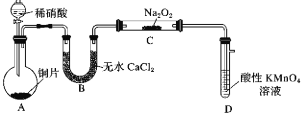
Ⅰ.某研究小组设计了一套制备及检验 SO2 部分性质的装置,如图 1 所示。
(1)仪器 A 的名称______________,导管 b 的作用______________。
(2)装置乙的作用是为了观察生成 SO2的速率,则装置乙中加入的试剂是______________。
(3)①实验前有同学提出质疑:该装置没有排空气,而空气中的 O2 氧化性强于 SO2,因此 装置丁中即使有浑浊现象也不能说明是 SO2 导致的。请你写出 O2 与 Na2S 溶液反应的化学 反应方程式______________。
②为进一步检验装置丁产生浑浊现象的原因,进行新的实验探究。实验操作及现象见表。
序号 | 实验操作 | 实验现象 |
1 | 向 10ml 1mol·L-1 的 Na2S 溶液中通 O2 | 15min 后,溶液才出现浑浊 |
2 | 向 10ml 1mol·L-1 的 Na2S 溶液中通 SO2 | 溶液立即出现黄色浑浊 |
由实验现象可知:该实验条件下 Na2S 溶液出现浑浊现象是 SO2 导致的。你认为上表实验 1 反应较慢的原因可能是______________。
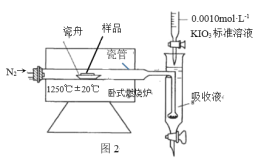
Ⅱ.铁矿石中硫元素的测定可以使用燃烧碘量法,其原理是在高温下将样品中的硫元素转化 为 SO2 , 以 淀 粉 和 碘 化 钾 的 酸 性 混 合 溶 液 为 SO2 吸 收 液 , 在 SO2 吸 收 的 同 时 用 0.0010mol·L-1KIO3 标准溶液进行滴定,检测装置如图 2 所示:
[查阅资料] ①实验进行 5min,样品中的 S 元素都可转化为 SO2
②2IO3-+5SO2+4H2O=8H++5SO42-+I2
③I2+SO2+2H2=2I-+SO42-+4H+
④IO3-+5I-+6H+=3I2+3H2O
(4)工业设定的滴定终点现象是______________。
(5)实验一:空白试验,不放样品进行实验,5min 后测得消耗标准液体积为 V1mL
实验二:加入 1g 样品再进行实验,5min 后测得消耗标准液体积为 V2mL
比较数据发现 V1 远远小于 V2,可忽略不计 V1。 测得 V2 的体积如表
序号 | 1 | 2 | 3 |
KIO3 标准溶液体积/mL | 10.02 | 9.98 | 10.00 |
该份铁矿石样品中硫元素的质量百分含量为______________。
【答案】蒸馏烧瓶 平衡分液漏斗与蒸馏烧瓶的压强,使液体顺利流下或平衡压强使液体顺利流下 饱和亚硫酸氢钠溶液 O2+2H2O+2Na2S==4NaOH+2S ↓ 氧气在水中的溶解度比二氧化硫小 吸收液出现稳定的蓝色 0.096%
【解析】
根据实验原理及实验装置分析解答;根据物质性质及氧化还原反应原理分析书写化学方程式;根据滴定原理分析解答。
(1)根据图中仪器构造及作用分析,仪器A为蒸馏烧瓶;导管b是为了平衡气压,有利于液体流出;故答案为:蒸馏烧瓶;平衡气压,有利于液体流出;
(2)装置B的作用之一是观察SO2的生成速率,其中的液体最好是既能观察气体产生的速率,也不反应消耗气体,SO2与饱和NaHSO3溶液不反应,也不能溶解,可以选择使用;故答案为:饱和NaHSO3溶液;
(3)①氧气与Na2S反应生成硫单质和氢氧化钠,化学反应方程式为:Na2S+O2=S↓+2NaOH;故答案为:Na2S+O2=S↓+2NaOH;
②氧气在水中的溶解度比二氧化硫小,导致上表实验1反应较慢,故答案为:氧气在水中的溶解度比二氧化硫小;
(4)可知滴定终点时生成了I2,故滴定终点现象为:溶液由无色变为蓝色,且半分钟溶液不变色。故答案为:溶液由无色变为蓝色,且半分钟溶液不变色;
(5)V(KIO3)=![]() ,根据滴定原理及反应中得失电子守恒分析,n(S)=n(SO2)=3 n(KIO3)= 3×0.0010mol·L-1×0.01L=3×10-5mol,则该份铁矿石样品中硫元素的质量百分含量为
,根据滴定原理及反应中得失电子守恒分析,n(S)=n(SO2)=3 n(KIO3)= 3×0.0010mol·L-1×0.01L=3×10-5mol,则该份铁矿石样品中硫元素的质量百分含量为![]() ,故答案为:0.096%。
,故答案为:0.096%。

 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案