题目内容
17.下列离子方程式书写正确的是( )| A. | 氯气与NaOH溶液反应:Cl2+OH-═Cl-+ClO-+H2O | |
| B. | 氢氧化铝与稀硫酸反应:OHˉ+H+═H2O | |
| C. | 铁粉加入稀硫酸中:2Fe+6H+═2Fe3++3H2↑ | |
| D. | 氯化铝溶液中加入过量氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ |
分析 A.电荷不守恒;
B.氢氧化铝不溶于水,应写成化学式;
C.铁与稀硫酸反应生成硫酸亚铁和氢气;
D.一水合氨为弱碱,与氯化铝反应生成氢氧化铝和氯化铵.
解答 解:A.电荷不守恒,应为Cl2+2OH-═Cl-+ClO-+H2O,故A错误;
B.氢氧化铝不溶于水,应写成化学式,反应的离子方程式为Al(OH)3+3H+═Al3++3H2O,故B错误;
C.铁与稀硫酸反应生成硫酸亚铁和氢气,离子方程式为Fe+2H+═Fe3++H2↑,故C错误;
D.一水合氨为弱碱,与氯化铝反应生成氢氧化铝和氯化铵,反应的离子方程式为Al3++3NH3•H2O═Al(OH)3↓+3NH4+,故D正确.
故选D.
点评 本题考查离子反应方程式的书写,明确物质之间反应的量的关系为解答的关键,注意离子反应的书写方法及沉淀、气体、水等保留化学式,题目难度不大.

练习册系列答案
相关题目
20.下列实验装置中正确的是( )
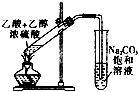

| A. | 实验室用液溴、苯和铁制备溴苯时必须加热 | |
| B. | 实验室可用如图所示装置进行酯化实验 | |
| C. | 如果甲烷中混有少量乙烯,可以通过盛有酸性KMnO4溶液进行除杂 | |
| D. | 将加热后的铜丝多次插入乙醇中,乙醇中可以闻到刺激性气味 |
8.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 22.4LNO与11.2LO2充分反应后,气体分子总数为NA | |
| B. | 常温下71gCl2与足量NaOH溶液反应,转移电子数为2NA | |
| C. | 25℃时,pH=13的Ba(OH)2溶液中含有的OH-数目为0.2NA | |
| D. | 将CO2通过Na2O2使其增重ag时,反应转移的电子数为$\frac{a{N}_{A}}{28}$ |
12.已知C-C键可以绕键轴自由旋转,结构简式为 的烃,下列说法中正确的是( )
的烃,下列说法中正确的是( )
 的烃,下列说法中正确的是( )
的烃,下列说法中正确的是( )| A. | 该烃属于苯的同系物 | |
| B. | 分子中至少有16个碳原子处于同一平面上 | |
| C. | 分子中至少有9个碳原子处于同一平面上 | |
| D. | 分子中至少有11个碳原子处于同一平面上 |
2.现有部分短周期元素的性质或原子结构如下表:
下列说法正确的是( )
| 元素编号 | 元素性质或原子结构 |
| T | 最外层电子数是次外层电子数的2倍 |
| X | L层有三个未成对电子 |
| Y | L层p电子数比s电子数多两个 |
| Z | 元素的最高正价为+7价 |
| A. | z离子的结构示意图为: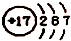 | B. | 分子TY2的键角为l80° | ||
| C. | X原子的轨道式为: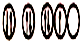 | D. | XZ3为非极性分子 |
6.下列物质属于有机物的是( )
| A. | 氰化钾(KCN) | B. | 碳酸氢钾(KHCO3) | C. | 乙炔(C2H2) | D. | 碳化硅(SiC) |
7.容量瓶上需标有①压强 ②浓度 ③容量 ④温度 ⑤刻度线 五项中的( )
| A. | ①②④ | B. | ①③⑤ | C. | ②③⑤ | D. | ③④⑤ |
 ,该化合物中化学键类型有离子键和共价键.
,该化合物中化学键类型有离子键和共价键.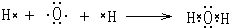 .
. .
.