题目内容
19.2g铜与适量的浓HNO3反应,铜全部反应后,共收集到11.2 LNO和NO2混合气体(标准状况),反应消耗HNO3的物质的量是( )
| A.0.8 mol | B.1.1 mol | C.1.2 mol | D.2.0 mol |
B
解析试题分析:Cu与硝酸反应,开始是浓硝酸,发生反应:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O;随着反应的进行,硝酸变稀,这时发生反应:3Cu+8HNO3(稀)=2Cu(NO3)2+2NO↑+4H2O。可见在反应中硝酸的作用有两个:一是形成Cu(NO3)2;二是得到电子变为气态氧化物NO、NO2。n(Cu)="m÷M" ="19.2g÷" 64g/mol=0.3mol.n(气体)=V÷Vm= 11.2 L÷22.4L/mol=0.5mol.所以n(HNO3)=2n(Cu)+ n(气体)="2×" 0.3mol+ 0.5mol=1.1mol。故选项为B。
考点:考查守恒法在化学计算中的应用的知识。

 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案根据表中信息,判断下列叙述中正确的是
| 序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
| ① | | FeBr2 | / | | Cl- |
| ② | MnO2 | 浓盐酸 | / | Cl2 | |
| ③ | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
A.表中①组的反应可能有一种或两种元素被氧化
B.氧化性强弱的比较:MnO2>Fe3+>Cl2>Br2
C.表中②组反应的氧化产物是MnCl2,1molMnO2电子转移数目是2NA
D.表中③组反应的离子方程式为:2MnO4—+3H2O2+6H+=2Mn2++4O2↑+6H2O
下列化工生产过程中发生的反应,不属于氧化还原反应的是
| A.用氨气制硝酸 | B.用石灰石制生石灰 |
| C.用氯气制漂白粉 | D.从卤水中提取溴单质 |
下列叙述中,金属a的活泼性肯定比金属b的活泼性强的是
| A.a原子的最外层电子数比b原子的最外层电子数少 |
| B.把a、b两块金属片浸入稀硫酸中,用导线相连组成原电池时,电流由 a到b |
| C.1mol a 从酸中置换H+生成的H2比1 mol b从酸中置换H+生成的H2多 |
| D.常温时,a能从水中置换出氢,而b不能 |
在含有n mol FeI2的溶液中通入Cl2,有x mol Cl2发生反应。下列说法正确的是
A.当x ≤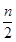 时,反应的离子方程式为:2Fe2++ Cl2 → 2Fe3++ 2Cl- 时,反应的离子方程式为:2Fe2++ Cl2 → 2Fe3++ 2Cl- |
| B.当x ≥ n时,反应的离子方程式为:2Fe2++ 2I-+ 2Cl2 → 2Fe3++ I2+ 4Cl- |
| C.当Fe2+和I-同时被氧化时,x与n的关系为x>n |
| D.当x=n时,反应后氧化产物的物质的量为n mol |
在2009年10月1日,新的饮用矿泉水强制性国家标准《饮用天然矿泉水》正式实施,其中“溴酸盐(BrO3-)”这一潜在致癌物质被做了严格限制。有关专家解释,矿泉水在开采过程中会含有少量溴化物(Br-),在后续的生产过程中经臭氧(O3)处理逐渐转化成溴酸盐。下列有关该转化过程的认识正确的是( )
| A.该过程中溴化物(Br-)得到电子 |
| B.该过程中臭氧(O3)是氧化剂,溴酸盐(BrO3-)是还原剂 |
| C.该过程中溴元素被还原,氧元素被氧化 |
| D.该过程中溴元素发生氧化反应,氧元素发生还原反应 |
向含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示。有关说法不正确的是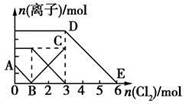
| A.线段BC代表Fe3+物质的量的变化情况 |
| B.原混合溶液中n(FeBr2)=3 mol |
| C.当通入2 mol Cl2时,溶液中已发生的离子反应可表示为: 2Fe2++2I-+2Cl2===2Fe3++I2+4Cl- |
| D.原溶液中n(Fe2+):n(I-):n(Br-)=3:1:2 |
从淡化海水中提取溴的流程如图所示,下列有关说法错误的是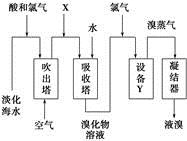
| A.X为SO2气体,也可将SO2换成Na2SO3 |
| B.设备Y为蒸馏塔 |
| C.在提取溴的过程中一定有Br-被氧化 |
| D.工业上每获得1 mol Br2,需要消耗Cl2的体积最多为44.8 L(标准状况下) |
已知常温下可用Co2O3制备Cl2,反应前后存在六种微粒:Co2O3、H2O、Cl2、H+、Cl-和Co2+。下列叙述不正确的是 ( )。
| A.氧化产物为Cl2 |
| B.参加反应的氧化剂与还原剂的物质的量之比为1∶2 |
| C.若有3 mol H2O生成,则反应中有2 mol电子转移 |
| D.当该反应生成2.24 L Cl2(标准状况)时,反应中有0.1 mol电子转移 |