题目内容
【题目】将x molA与y mol B充入密闭容器中发生如下反应:xA(g)+yB(g)![]() zC(g);ΔH=-akJ·mol-1(a>0)
zC(g);ΔH=-akJ·mol-1(a>0)
在某温度下达到平衡状态,请回答下列问题:
(1)若减压后v正<v逆,则x、y、z的关系是____。
(2)若恒温、恒压下向原平衡中加入C,则平衡_____移动(填“正向”、“逆向”或“不”),重新达平衡后C的体积分数_____(填“增大”、“减小”或“不变”)。
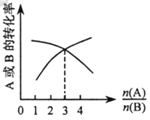
(3)如图,纵坐标为反应物的转化率,横坐标是反应物初始用量之比![]() ,则x∶y =___;
,则x∶y =___;![]() 一定时,平衡状态A的转化率在恒温条件下比在绝热环境中是高还是低?____。
一定时,平衡状态A的转化率在恒温条件下比在绝热环境中是高还是低?____。
(4)恒温、恒容下,x mol A与y mol B反应达到平衡时能量变化为a1 kJ,xmolA与1.5ymolB反应达到平衡时能量变化为a2kJ,则a、a1、a2、由大到小顺序为____。(a、a1、a2均大于0)
【答案】x+y>z 逆向 不变 3∶l 高 a>a2>a1
【解析】
将x molA与y mol B充入密闭容器中发生如下反应:xA(g)+yB(g)![]() zC(g);ΔH=-akJ·mol-1(a>0) 在某温度下达到平衡状态,请回答下列问题:
zC(g);ΔH=-akJ·mol-1(a>0) 在某温度下达到平衡状态,请回答下列问题:
(1)减小压强,平衡向气体总物质的量增大的方向移动;
(2)增大反应物的量,平衡逆向移动;在恒温、恒压下向原平衡中加入C,重新形成的平衡与平衡等效;
(3)反应物的起始物质的量之比等于化学计量数之比时,反应物的转化率相等;如图,当![]() =3时,A的转化率和B的转化率相等;
=3时,A的转化率和B的转化率相等;![]() 一定时,温度升高平衡向吸热反应方向移动;
一定时,温度升高平衡向吸热反应方向移动;
(4)可逆反应,反应物的转化率始终小于100%;增大反应物的量,平衡正向移动。
将x molA与y mol B充入密闭容器中发生如下反应:xA(g)+yB(g)![]() zC(g);ΔH=-akJ·mol-1(a>0) 在某温度下达到平衡状态,请回答下列问题:
zC(g);ΔH=-akJ·mol-1(a>0) 在某温度下达到平衡状态,请回答下列问题:
(1)减小压强,平衡向气体总物质的量增大的方向移动,若减压后v正<v逆,说明平衡逆向移动,即逆方向是气体总物质的量增大的方向,即x、y、z的关系是x+y>z;
(2)增大反应物的量,平衡逆向移动;则在恒温、恒压下向原平衡中加入C,平衡逆向移动,重新形成的平衡与平衡等效,即C的体积分数不变;
(3)反应物的起始物质的量之比等于化学计量数之比时,反应物的转化率相等;如图,当![]() =3时,A的转化率和B的转化率相等,即x∶y =3:1;已知xA(g)+yB(g)
=3时,A的转化率和B的转化率相等,即x∶y =3:1;已知xA(g)+yB(g)![]() zC(g);ΔH=-akJ·mol-1(a>0),
zC(g);ΔH=-akJ·mol-1(a>0),![]() 一定时,反应在绝热条件下进行,容器内温度升高,相对恒温条件下的平衡状态,平衡逆向移动,则温度升高平衡向吸热反应方向移动,平衡状态A的转化率在恒温条件下比在绝热环境中高;
一定时,反应在绝热条件下进行,容器内温度升高,相对恒温条件下的平衡状态,平衡逆向移动,则温度升高平衡向吸热反应方向移动,平衡状态A的转化率在恒温条件下比在绝热环境中高;
(4)恒温、恒容下,已知xA(g)+yB(g)![]() zC(g);ΔH=-akJ·mol-1(a>0),则当xmol的A完全反应时反应放出的热量为akJ; x mol A与y mol B反应达到平衡时能量变化为a1 kJ, xmolA与1.5ymolB反应达到平衡时A的转化率比x mol A与y mol B反应达到平衡时转化率大,则能量变化为a2kJ>a1kJ,因xmolA不能完全转化,则放出的能量小于akJ;即a>a2>a1。
zC(g);ΔH=-akJ·mol-1(a>0),则当xmol的A完全反应时反应放出的热量为akJ; x mol A与y mol B反应达到平衡时能量变化为a1 kJ, xmolA与1.5ymolB反应达到平衡时A的转化率比x mol A与y mol B反应达到平衡时转化率大,则能量变化为a2kJ>a1kJ,因xmolA不能完全转化,则放出的能量小于akJ;即a>a2>a1。

 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案