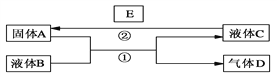
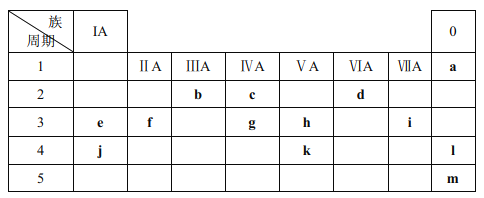
��Ŀ����
����Ŀ���� NAΪ�����ӵ���������ֵ�������й�������ȷ����( )
A. 100g ��������Ϊ 46%���Ҵ�(C2H5OH)��Һ�к���ԭ������Ϊ 4NA
B. ��״���£� 2.24 L CCl4 ���еĹ��ۼ���Ϊ 0.4NA
C. 1 L 0.1 mol��L-1 ������(CH3COOH)��Һ�к� H+������Ϊ 0.1NA
D. 235g����23592U�����ѱ䷴Ӧ: ![]() ��������������(
��������������(![]() )��Ϊ10NA
)��Ϊ10NA
���𰸡�A
��������A���ֱ�������ʺ��ܼ��к��е���ԭ������B.CCl4�ڱ����ΪҺ̬�������㣻C.������Һ��ˮҲ����������ӣ�D.�����ѱ䷴Ӧ����ʽ������
A��ܼ�ˮ�к�����ԭ�ӣ�100g46%�ƾ�ˮ��Һ��C2H5OHΪ46g�����ʵ���Ϊ1mol,���к�����ԭ����ΪNA���ܼ�ˮΪ54g�����ʵ���Ϊ3mol�����к�����ԭ��3NA������100g ��������Ϊ 46%���Ҵ�(C2H5OH)��Һ�к���ԭ������Ϊ 4NA����A��ȷ��
B.CCl4�ڱ����ΪҺ̬�������������ʵ�������B����
C.������Һ��ˮҲ����������ӣ���C����
D�235g����![]() �����ʵ���Ϊ1mol�����ݷ�Ӧ����ʽ��֪����Ӧ����Ҫ
�����ʵ���Ϊ1mol�����ݷ�Ӧ����ʽ��֪����Ӧ����Ҫ![]() ����1mol
����1mol![]() �����������ӣ�
�����������ӣ�![]() ����Ϊ9 NA����D�����
����Ϊ9 NA����D�����
����������������ȷ��ΪA��

 ������ĩ��ϰ��ѵ��ϵ�д�
������ĩ��ϰ��ѵ��ϵ�д� С��ʿ��ĩ����100��ϵ�д�
С��ʿ��ĩ����100��ϵ�д�����Ŀ����1����2L�����ܱ������У�������Ӧ2NO��g��+O2��g��2NO2��g����
��ij�¶�ʱ�������ʵ�����2��1����NO��O2��ʼ��Ӧ��n��NO����ʱ��仯�����
ʱ�䣨s�� | 0 | 1 | 2 | 3 | 4 | 5 |
n��NO����mol�� | 0.020 | 0.010 | 0.007 | 0.006 | 0.006 | 0.006 |
0��4s����O2Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ________��
����˵���÷�Ӧ�Ѵﵽƽ��״̬����________��
A��������ɫ���ֲ��� B������ƽ����Է����������ֲ���
C��������NO��=2������O2�� D������ѹǿ���ֲ���
����֪��K300�棾K400�森���д�ʩ��ʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ�����_______��
A�������¶� B������Arʹѹǿ����
C��ѡ���Ч���� D������NOʹѹǿ����
��2������ȼ�ϵ�ؿ����������������ʣ���ͼ�����ü���ȼ�ϵ�ص��100ml 1mol/Lʳ��ˮ�����һ��ʱ����ռ�����״���µ�����2.24L���������Һ������䣩��
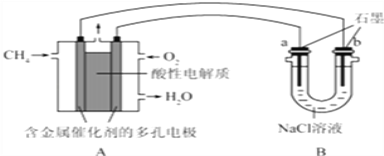
�ټ���ȼ�ϵ�صĸ�����Ӧʽ��____________________________________________��
�ڵ�����Һ��pH=________����������������������Һ��Ӧ����
��3���ڻ�ѧ��Ӧ�У�ֻ�м�����������ƽ�������ߵö�ķ�Ӧ����ӷ�����ײʱ�ſ��ܷ�����ѧ��Ӧ����Щ���ӳ�Ϊ����ӣ�ʹ��ͨ���ӱ�ɻ���������ṩ������ȵ������л�ܣ��䵥λͨ����kJ/mol��ʾ��������۲���ͼ��Ȼ��ش����⣺

������3����Ӧ�з���ʾ��ͼ�����ķ�Ӧ���� ___________������ţ���
A��������Fe2O3��Ӧ B����ˮϡ��Ũ������Һ C�����ȵ�̼��CO2��Ӧ
���Լ���Ϊԭ����ȡ�����ǹ�ҵ�ϳ��õ����ⷽ������֪��
CH4��g��+H2O��g��=CO��g��+3H2��g����H=+306kJ/mol
CH4��g��+CO2��g��=2CO��g��+2H2��g����H=+240kJ/mol
CH4��g����H2O��g����Ӧ����CO2��g����H2��g�����Ȼ�ѧ����ʽΪ_______________________��