题目内容
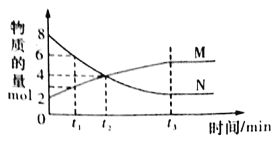
【题目】常温下,0.2mol·L-1的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是

A.HA为强酸
B.该混合液pH=7
C.图中X表示HA,Y表示OH-,Z表示H+
D.该混合溶液中:c(A-)+c(Y)=c(Na+)
【答案】D
【解析】
试题分析:A、0.2 mol/L一元酸HA与等浓度的NaOH溶液等体积混合,恰好反应得到0.1 mol/L的NaA溶液,若HA为强酸,则溶液为中性,且c(A-)=0.1 mol/L,与图不符,所以HA为弱酸,A错误;B、根据A的分析,NaA是强碱弱酸盐,溶液的pH>7,B项误;C、A-水解使溶液显碱性,所以溶液中的粒子浓度的大小关系是c(Na+)>c(A-)>c(OH-)>c(HA)>c(H+),所以X是OH-,Y是HA,Z表示H+,C错误;D、根据物料守恒,有c(A-)+c(HA)=c(Na+),D正确;答案选D。

练习册系列答案
相关题目
【题目】已知硫代硫酸钠溶液与稀H2SO4反应可析出单质硫沉淀:Na2S2O3+H2SO4===Na2SO4+S↓+SO2↑+H2O,某同学按下表进行实验,请你判断哪一组先出现浑浊。
编号 | 加3%Na2S2O3/mL | 加1∶5的H2SO4/滴 | 温度/℃ |
1 | 5 | 25 | 25 |
2 | 5 | 15 | 35 |
3 | 5 | 25 | 45 |