题目内容
已知反应Zn+2AgNO3═Zn(NO3)2+2Ag选择适宜的材料和试剂将该反应设计成一个原电池.
(1)画出装置图,并注明电池的正、负极及电极材料和电解质溶液: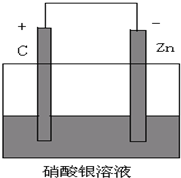

(2)写出电极反应式:
(1)画出装置图,并注明电池的正、负极及电极材料和电解质溶液:


(2)写出电极反应式:
正极:2Ag++2e-═2Ag(或Ag++e-═Ag);负极:Zn-2e-═Zn2+
正极:2Ag++2e-═2Ag(或Ag++e-═Ag);负极:Zn-2e-═Zn2+
.分析:利用反应Zn+2AgNO3═Zn(NO3)2+2Ag设计原电池时,根据反应可知,Zn为负极,则正极可以是活泼性不如Zn的金属如Cu等,也可以是碳棒,电解质溶液应为AgNO3,工作时,正极反应式为2Ag++2e-═2Ag,负极反应式为Zn-2e-═Zn2+,Zn棒逐渐溶解.
解答:解:(1)利用反应Zn+2AgNO3═Zn(NO3)2+2Ag设计原电池时,根据反应可知,Zn为负极,则正极可以是活泼性不如Zn的金属如Cu等,也可以是碳棒,电解质溶液应为AgNO3,
故答案为: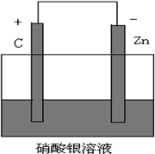 ;
;
(2)正极上银得电子发生还原反应,电极反应式为:2Ag++2e-═2Ag(或Ag++e-═Ag),负极上锌失电子发生氧化反应,电极反应式为:Zn-2e-═Zn2+,
故答案为:2Ag++2e-═2Ag(或Ag++e-═Ag);Zn-2e-═Zn2+.
故答案为:
 ;
;(2)正极上银得电子发生还原反应,电极反应式为:2Ag++2e-═2Ag(或Ag++e-═Ag),负极上锌失电子发生氧化反应,电极反应式为:Zn-2e-═Zn2+,
故答案为:2Ag++2e-═2Ag(或Ag++e-═Ag);Zn-2e-═Zn2+.
点评:本题考查原电池的设计和工作原理,题目难度不大,注意原电池正负极材料及电解质溶液的选择.

练习册系列答案
相关题目

 和I-发生反应的离子方程式为:
和I-发生反应的离子方程式为: 和I-发生反应的离子方程式为:
和I-发生反应的离子方程式为: