题目内容
下列物质中既含有共价键又含有离子键的是
- A.NaI
- B.CaCl2
- C.NO2
- D.KNO3
D
一般活泼的金属和活泼的非金属容易形成离子键,非金属元素的原子间形成共价键。碘化钠、氯化钙含有的均是离子键。NO2含有的是极性键,在硝酸钾中含有的化学键有离子键,同时氮和氧之间还有极性键,所以答案选D。
一般活泼的金属和活泼的非金属容易形成离子键,非金属元素的原子间形成共价键。碘化钠、氯化钙含有的均是离子键。NO2含有的是极性键,在硝酸钾中含有的化学键有离子键,同时氮和氧之间还有极性键,所以答案选D。

练习册系列答案
 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目

 在下列化合物中:H2O2 、Na2O、、I2 、、NaCl、、CO2、NH4Cl、Na2O2,用化学式回答下列问题:
在下列化合物中:H2O2 、Na2O、、I2 、、NaCl、、CO2、NH4Cl、Na2O2,用化学式回答下列问题: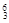 Li ②
Li ②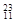 Na ③
Na ③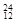 Mg ④
Mg ④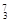 Li ⑤
Li ⑤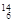 C ⑥C60 ⑦石墨,为同位素的是 ,互为同素异形体的是 。(填编号)
C ⑥C60 ⑦石墨,为同位素的是 ,互为同素异形体的是 。(填编号)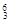 Li ②
Li ②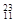 Na ③
Na ③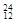 Mg ④
Mg ④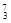 Li ⑤
Li ⑤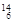 C ⑥C60 ⑦石墨,为同位素的是 ,互为同素异形体的是 。(填编号)
C ⑥C60 ⑦石墨,为同位素的是 ,互为同素异形体的是 。(填编号)