题目内容
电子计算器所用的纽扣式电池为银锌电池,其电极分别为Ag2O和Zn,电解质溶液为KOH溶液,电极反应为Zn+2OH--2e-=Zn(OH)2、Ag2O+H2O+2e-=2Ag+2OH-.下列叙述中,不正确的是( )
分析:根据化合价变化可知Zn被氧化,应为原电池的负极,则正极为Ag2O,原电池中电流从正极流向负极,根据电极反应式可得电池总反应为Zn+Ag2O=ZnO+2Ag.
解答:解:A、由电极反应式可知,Zn的化合价由0价升高到+2价,被氧化,为原电池的负极,则正极为Ag2O,原电池中电子从负极流向正极,即从锌经导线流向Ag2O,故A正确;
B、由电极反应式可知,Zn的化合价由0价升高到+2价,为原电池的负极,发生氧化反应,Ag2O是正极发生还原反应,故B错误;
C、由电极反应式可知,Zn的化合价由0价升高到+2价,为原电池的负极,发生氧化反应,Ag2O是正极发生还原反应,故C正确;
D、负极电极反应为Zn+2OH-=ZnO+H2O+2e-,消耗氢氧根离子,溶液的pH减小,正极电极反应为:Ag2O+H2O+2e-=2Ag+2OH-,生成氢氧根离子,该区域溶液的pH增大,故D正确.
故选B.
B、由电极反应式可知,Zn的化合价由0价升高到+2价,为原电池的负极,发生氧化反应,Ag2O是正极发生还原反应,故B错误;
C、由电极反应式可知,Zn的化合价由0价升高到+2价,为原电池的负极,发生氧化反应,Ag2O是正极发生还原反应,故C正确;
D、负极电极反应为Zn+2OH-=ZnO+H2O+2e-,消耗氢氧根离子,溶液的pH减小,正极电极反应为:Ag2O+H2O+2e-=2Ag+2OH-,生成氢氧根离子,该区域溶液的pH增大,故D正确.
故选B.
点评:本题考查原电池知识,题目难度不大,注意根据电极反应判断原电池的正负极以及电池反应.

练习册系列答案
相关题目
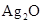 ,电解质溶液为KOH溶液;其电极反应分别是:
,电解质溶液为KOH溶液;其电极反应分别是: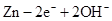 ══
══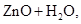
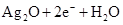 ══
══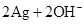 。下列叙述正确的是( )
。下列叙述正确的是( )