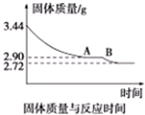
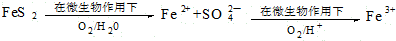题目内容
化学反应的重要应用之一是制备新物质。Ⅰ.实验室通常用二氧化锰和浓盐酸反应制取Cl2。
(1)该反应的离子方程式为____________________________________________。
(2)甲、乙两同学用下列两种方法制取氯气:
甲:用含HCl 146 g的浓盐酸与足量二氧化锰反应 乙:用87 g二氧化锰与足量浓盐酸反应
则二者制得的Cl2(填序号)___________。
①甲比乙多 ②乙比甲多 ③一样多 ④无法比较
Ⅱ.已知下列反应也可以生成氯气:
①2KMnO4+16HCl(浓)![]() 2KCl+2MnCl2+5Cl2↑+8H2O ②4HCl+O2
2KCl+2MnCl2+5Cl2↑+8H2O ②4HCl+O2![]() 2Cl2+2H2O ③2NaCl+2H2O
2Cl2+2H2O ③2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
其中,适宜于实验室制取Cl2的反应是_____________(填序号,下同),适宜于工业上生产Cl2的反应是_____________。
Ⅰ.(1)MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
(2)②
Ⅱ.① ③
解析:理论上看,146 gHCl与87 g MnO2恰好能完全反应,但随着反应的进行,盐酸浓度减小后,将不再与MnO2反应,故87 gMnO2与足量的浓盐酸反应放出的Cl2多。因反应②需催化剂,反应③条件是电解,故实验室常用反应①来制取Cl2,而工业上则通常用电解法。

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案
相关题目
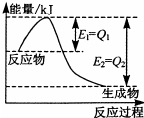 运用化学反应原理研究氮、硫、氯等单质及其化合物的反应有重要的意义.
运用化学反应原理研究氮、硫、氯等单质及其化合物的反应有重要的意义.