题目内容
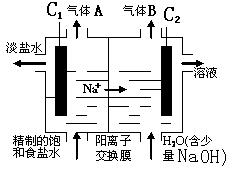
以电解饱和食盐水为基础制取氯气等产品的工业称为“氯碱工业”,它是目前化学工业的重要支柱之一.
(1)请写出电解饱和食盐水制备氯气的化学反应原理,并用“双线桥法”标出电子转移的方向和数目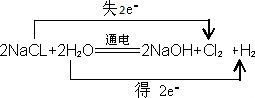

(2)工业上用电解饱和食盐水得到的产物来生产消毒液(主要成分是NaClO),其反应的化学方程式为:
(1)请写出电解饱和食盐水制备氯气的化学反应原理,并用“双线桥法”标出电子转移的方向和数目


(2)工业上用电解饱和食盐水得到的产物来生产消毒液(主要成分是NaClO),其反应的化学方程式为:
2NaOH+Cl2═NaCl+NaClO+H2O
2NaOH+Cl2═NaCl+NaClO+H2O
,该反应中氧化剂和还原剂的物质的量之比为1:1
1:1
.分析:(1)电解饱和食盐水生成氢氧化钠、氯气和氢气,依据元素化合价变化标注电子转移;
(2)电解饱和食盐水得到的产物来生产消毒液是氯气和氢氧化钠溶液反应生成次氯酸钠、氯化钠和水,反应中氯元素化合价从-1价变化为0价,氢元素化合价从+1价变化为0价,依据电子转移守恒计算氧化剂和还原剂的物质的量之比;
(2)电解饱和食盐水得到的产物来生产消毒液是氯气和氢氧化钠溶液反应生成次氯酸钠、氯化钠和水,反应中氯元素化合价从-1价变化为0价,氢元素化合价从+1价变化为0价,依据电子转移守恒计算氧化剂和还原剂的物质的量之比;
解答:解:(1)电解饱和食盐水生成氢氧化钠、氯气和氢气,氯元素化合价从-1价变化为0价,氢元素化合价从+1价变化为0价,反应过程中电子转移总数为2;依据双线桥法标注电子转移为: ;
;
故答案为: ;
;
(2)电解饱和食盐水得到的产物来生产消毒液是氯气和氢氧化钠溶液反应生成次氯酸钠、氯化钠和水,反应的化学方程式为:2NaOH+Cl2═NaCl+NaClO+H2O;反应中氯元素化合价从-1价变化为0价,氢元素化合价从+1价变化为0价,依据电子转移守恒计算氧化剂和还原剂的物质的量之比1;1;
故答案为:1:1;
 ;
;故答案为:
 ;
;(2)电解饱和食盐水得到的产物来生产消毒液是氯气和氢氧化钠溶液反应生成次氯酸钠、氯化钠和水,反应的化学方程式为:2NaOH+Cl2═NaCl+NaClO+H2O;反应中氯元素化合价从-1价变化为0价,氢元素化合价从+1价变化为0价,依据电子转移守恒计算氧化剂和还原剂的物质的量之比1;1;
故答案为:1:1;
点评:本题考查了氧化还原反应电子转移标注方法,氧化还原反应中氧化剂还原剂的定量计算,题目较简单.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
 氢气是一种清洁能源,可以通过多种方法制得.
氢气是一种清洁能源,可以通过多种方法制得.


 s) + H2O(g)
s) + H2O(g)  CO(g) + H2(g) △H> 0
CO(g) + H2(g) △H> 0