题目内容
实验室配制100mL 1.00mol/L的硫酸溶液,回答下列问题:
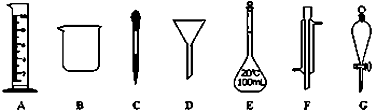
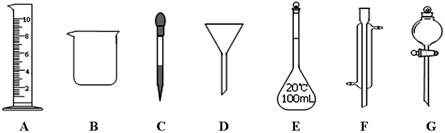
⑴所需98%的浓硫酸(ρ= 1.84g/mL)的体积是 mL。(精确到小数点后一位)。量取时应选择最大量程为 mL的量筒。
A、5 B、10 C、20 D、100
⑵配制过程和主要步骤依次是:A、量取 B、溶解 C、转液 D、
E、 F、摇匀等操作。
⑶、步骤B的操作方法是
。
进行该操作后, (“能”或“不能”)马上进行操作C,理由是
。
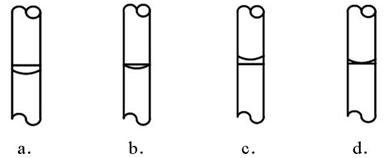
⑷上述⑵中E操作的方法是
。
⑸操作B、C均要用到的玻璃仪器是 ,若进行C操作时未用该仪器,导致有溶液外流,出现这种情况后,正确的处理方法是 。
⑹将浓硫酸按所需体积准确量取后,在空气中放置一段时间后再进行B、C、D、E、F操作,则所配硫酸溶液的浓度将 (“大于”或“等于”或“小于”)1.00mol/L。
⑴5.4;B ⑵洗涤、定容
⑶将烧杯中先装约30mL水,然后沿烧杯内壁倒入浓硫酸,边倒边搅拌; 不; 浓硫酸溶解时放热,而执煌溶液不能马上倒入容量瓶中。
⑷先加水到离刻度2~3cm处,然后改用胶头滴管加水到凹液面恰与刻度相切
⑸玻璃棒;重新配制 ⑹ ==

| A、用托盘天平称取10.6g Na2CO3固体 | B、将Na2CO3固体放入容量瓶中,加水至刻度线 | C、定容时俯视液面,所得溶液浓度偏低 | D、加水时不慎超过刻度线,用胶头滴管直接吸出多余液体 |