题目内容
【题目】乙烯是石油化学工业最重要的基础原料,经乙烯为原料可以制得许多工业材料和日用品。乙烯能发生下列转化关系:
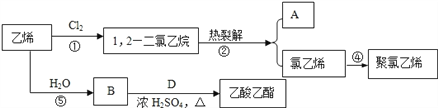
(1)A的分子式为____________,化合物D的官能团名称是_____________。反应⑤的反应类型为______________________。
(2)写出反应①、④的化学方程式(不用写反应条件)
①________________________;
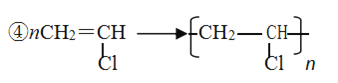
④________________________。
(3)上述反应中,以生成有机产物为目标,原子利用率100%的反应有①和_____________。
(4)实验室用如图所示装置制备乙酸乙酯。
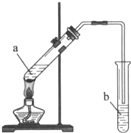
①试管a中生成乙酸乙酯的化学方程式是_____________________________。
②试管a中试剂的添加顺序是先加入_______,再加入_______,最后加入乙酸。浓硫酸的作用是做催化剂和_____________。
③试管b中盛放的试剂是________________,导气管不伸入液面下的理由是___________。
【答案】 HCl 羧基 加成 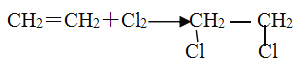
 ④和⑤(答道其中一个得分) CH3COOH+CH3CH2OH
④和⑤(答道其中一个得分) CH3COOH+CH3CH2OH ![]() CH3COOCH2CH3+H2O(无条件扣1分) 乙醇 浓硫酸 吸水剂 饱和Na2CO3溶液(无饱和也得分) 防止倒吸
CH3COOCH2CH3+H2O(无条件扣1分) 乙醇 浓硫酸 吸水剂 饱和Na2CO3溶液(无饱和也得分) 防止倒吸
【解析】乙烯与水发生加成反应生成B为CH3CH2OH,乙醇与D发生酯化反应生成乙酸乙酯,故D为CH3COOH;乙烯与氯气发生加成反应生成1,2-二氯乙烷,1,2-二氯乙烷发生热裂解得到A与氯乙烯,则A为HCl,氯乙烯发生加聚反应生成聚氯乙烯。
(1)由上述分析可知,A的分子为HCl,化合物D为CH3COOH,官能团名称是:羧基,故答案为:HCl;羧基;
(2)反应①是乙烯与氯气发生加成反应生成1,2-二氯乙烷,反应方程式为:CH2=CH2+Cl2→CH2Cl-CH2Cl,反应④是氯乙烯发生加聚反应生成聚氯乙烯,反应化学方程式为:n CH2=CHCl→ ,故答案为:CH2=CH2+Cl2→CH2Cl-CH2Cl;n CH2=CHCl→
,故答案为:CH2=CH2+Cl2→CH2Cl-CH2Cl;n CH2=CHCl→ ;
;
(3)加成反应中原子利用率为100%,上述反应中①④⑤属于加成反应,以生成有机产物为目标,原子利用率100%的反应有①和④⑤,故答案为:④⑤;
(4)①酯化反应的本质为酸脱羟基,醇脱氢,乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,该反应为可逆反应,反应的化学方程式为:CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O,故答案为:CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O,故答案为:CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O;
CH3COOCH2CH3+H2O;
②浓硫酸溶于水放出大量的热,乙醇中含有少量水,应将浓硫酸加入到乙醇中,防止硫酸溶解时放出大量的热导致液体飞溅,则加入药品的顺序为先在大试管中注入乙醇,再分别缓缓加入浓硫酸和乙酸(乙酸和浓硫酸的加入顺序可互换),边加边振荡试管使之混合均匀,即加入顺序为乙醇、浓硫酸、乙酸,浓硫酸的作用是做催化剂和吸水剂,故答案为:乙醇;浓硫酸;吸水剂;
③乙酸乙酯不溶于饱和碳酸钠溶液,乙醇易溶于水,乙酸可与碳酸钠发生反应而被吸收,用饱和碳酸钠溶液可将乙酸乙酯和乙醇、乙酸分离,反应的化学方程式为 2CH3COOH+Na2CO3→2CH3COONa+CO2↑+H2O;挥发出的乙酸、乙醇易溶于水,导气管下端管口不能浸入液面插入溶液中防止倒吸,导管要插在饱和碳酸钠溶液的液面上,伸入液面下会发生倒吸,故答案为:饱和碳酸钠溶液;防止倒吸。

 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案