题目内容
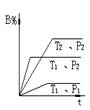
已知某可逆反应mA(g) + n B(g)  pC(g)+ Q在密闭容器中进行,图中表示在不同反应时间t时,温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析下列判断正确的( )
pC(g)+ Q在密闭容器中进行,图中表示在不同反应时间t时,温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析下列判断正确的( )
 pC(g)+ Q在密闭容器中进行,图中表示在不同反应时间t时,温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析下列判断正确的( )
pC(g)+ Q在密闭容器中进行,图中表示在不同反应时间t时,温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析下列判断正确的( )
| A.T1 < T2 P1 > P2 m + n >p Q < 0 |
| B.T1 > T2 P1 < P2 m + n >p Q < 0 |
| C.T1 < T2 P1 > P2 m + n <p Q > 0 |
| D.T1 > T2 P1 < P2 m + n <p Q < 0 |
D
温度越高,速率越快,图像越陡,故T1>T2;温度升高B%减小,故平衡正向移动,正向吸热,故Q<0;压强越大,速率越快,图像越陡,故P2>P1;压强增大B%增大,故平衡逆向移动,逆向体积减小,故m + n <p。

练习册系列答案
相关题目
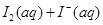

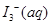
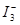 的物质的量浓度c(
的物质的量浓度c(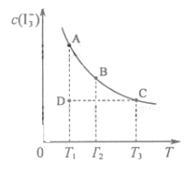
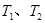 ,反应的平衡常数分别为
,反应的平衡常数分别为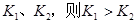
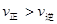
 2C(g)的下列叙述中,能说明反应已达到平衡的是( )
2C(g)的下列叙述中,能说明反应已达到平衡的是( )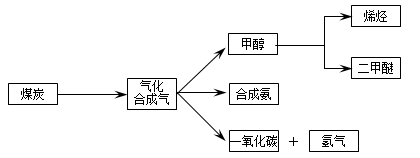
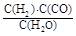 ,它所对应反应的化学方程式为 。
,它所对应反应的化学方程式为 。 温度230~280℃)进行下列反应:
温度230~280℃)进行下列反应: CH3OH(g) △H1=-90.7kJ·mol-1
CH3OH(g) △H1=-90.7kJ·mol-1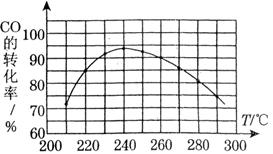
 。
。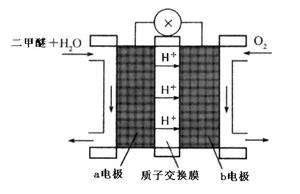
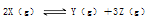
 向___(填“左”“右”或“不”,下同)移动;若将达到(1)的平衡体系中移走部分混合气体,则平衡向___移动。
向___(填“左”“右”或“不”,下同)移动;若将达到(1)的平衡体系中移走部分混合气体,则平衡向___移动。 H2(g)+I2(g)达到平衡后,下列说法中,正确的是:
H2(g)+I2(g)达到平衡后,下列说法中,正确的是:
 7N2+12H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是 L 。
7N2+12H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是 L 。 2SO3(g) ΔH =" -" 196.6 kJ· mol-1
2SO3(g) ΔH =" -" 196.6 kJ· mol-1