题目内容
MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如右图所示。下列叙述中正确的是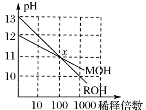
| A.在x点时,ROH完全电离 |
| B.在x点时,c(M+)>c(R+) |
| C.MOH是一种强碱 |
| D.稀释前,c(ROH)=10c(MOH) |
A
解析试题分析:从图中可以看出,ROH稀释100倍,pH降低2,说明是强电解质,完全电离,A项正确;在x点时,pH值相等,则氢离子、氢氧根离子浓度相等,M离子和R离子浓度相等,B项错误;MOH不能完全电离,C项错误;因为MOH是弱电解质,大量没有电离,物质的量浓度大于0.01mol/L,不能确定c(ROH)与10c(MOH)的关系。
考点:考查弱电解质的电离及稀释问题。
点评:通过图像要分析出是否稀释10倍,pH值下降1,来比较强弱电解质,属于简单题。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 (2011?崇明县一模)如图,MOH和ROH两种一元碱的稀溶液,分别加水稀释时pH变化可近似看作下图,下列说法错误的是( )
(2011?崇明县一模)如图,MOH和ROH两种一元碱的稀溶液,分别加水稀释时pH变化可近似看作下图,下列说法错误的是( ) MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如图所示.下列叙述中正确的是( )
MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如图所示.下列叙述中正确的是( ) MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化.如右图所示.下列叙述中正确的是( )
MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化.如右图所示.下列叙述中正确的是( ) (2011?焦作一模)MOH和ROH两种一元碱的稀溶液,分别加水稀释时pH变化可近似看作如图所示,下列说法错误的是( )
(2011?焦作一模)MOH和ROH两种一元碱的稀溶液,分别加水稀释时pH变化可近似看作如图所示,下列说法错误的是( ) 常温下MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如图所示.下列叙述中不正确的是( )
常温下MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如图所示.下列叙述中不正确的是( )