题目内容
下列实验操作能达到实验目的的是
| A.检验SO42-离子的存在:在未知溶液中加入BaCl2溶液产生白色沉淀,再加入稀硝酸沉淀不消失 |
| B.检验Fe2+:向某溶液中加入2滴KSCN溶液,溶液不显红色。再向溶液中加入几滴新制的氯水,溶液变为红色,说明原溶液一定含有Fe2+ |
| C.检验某气体是SO2:将某未知气体通入到品红溶液中,溶液褪色,则该气体一定是SO2 |
| D.检验CO32-:在某未知溶液中加入盐酸产生无色无味的能使澄清石灰水变浑浊的气体,则一定含有CO32- |
B
A中如果是Ag+的溶液加入氯化钡溶液也同样会产生不溶于硝酸的白色沉淀;C选项中也可能是其他的气体,如氯气、臭氧等;D选项中加入盐酸能产生CO2气体的可能是CO32-也可能是HCO3-。

练习册系列答案
 优等生题库系列答案
优等生题库系列答案
相关题目
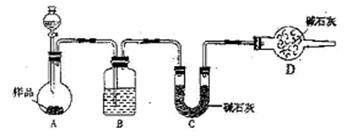
 Fe2O3+SO3↑SO3↑+14H2O↑,就设计了如下实验装置来验证绿矾受热分解是否发生上述反应。
Fe2O3+SO3↑SO3↑+14H2O↑,就设计了如下实验装置来验证绿矾受热分解是否发生上述反应。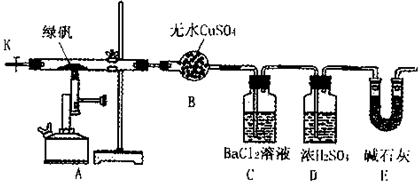
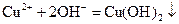 ,将
,将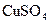 溶液滴入氨水中,振荡,会产生蓝色沉淀
溶液滴入氨水中,振荡,会产生蓝色沉淀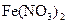 溶液中存在平衡:
溶液中存在平衡: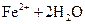
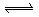
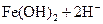 ,加入少量稀盐酸后溶液浅绿色会加深
,加入少量稀盐酸后溶液浅绿色会加深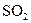 有漂白性,将
有漂白性,将