题目内容
已知CH3CH═CHCH3
2CH3CHO,则化学式为C5H10的烯烃在此条件下可生成醛的种类为( )
| [O] |
| A、5种 | B、4种 | C、3种 | D、6种 |
考点:同分异构现象和同分异构体
专题:同分异构体的类型及其判定
分析:根据题目信息可知烯烃氧化生成醛,双键的碳原子上至少连有1个氢原子,再根据烯烃的同分异构体判断,根据碳链缩短法书写C5H10的烯烃同分异构体,①先写烷烃同分异构体(烷烃碳骨架)②主链从长到短、支链由整到散、位置由心到边③“C=C”位置移动;
解答:
解:戊烷的同分异构体有CH3-CH2-CH2-CH2-CH3、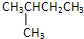 、
、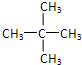 .
.
若为CH3-CH2-CH2-CH2-CH3,相应烯烃有CH2═CH-CH2-CH2-CH3、CH3-CH═CH-CH2-CH3;CH2═CH-CH2-CH2-CH3氧化生成甲醛、丁醛,CH3-CH═CH-CH2-CH3氧化生成乙醛、丙醛;
若为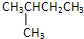 ,相应烯烃有:CH2═C(CH3)CH2CH3;CH3C(CH3)═CHCH3;CH3CH(CH3)CH═CH2;CH2═C(CH3)CH2CH3氧化可生成甲醛,CH3C(CH3)═CHCH3氧化生成乙醛,CH3CH(CH3)CH═CH2氧化可生成甲醛和2-甲基丙醛,
,相应烯烃有:CH2═C(CH3)CH2CH3;CH3C(CH3)═CHCH3;CH3CH(CH3)CH═CH2;CH2═C(CH3)CH2CH3氧化可生成甲醛,CH3C(CH3)═CHCH3氧化生成乙醛,CH3CH(CH3)CH═CH2氧化可生成甲醛和2-甲基丙醛,
若为 ,没有相应烯烃;
,没有相应烯烃;
所以化学式为C5H10的烯烃在此条件下可生成醛的种类为5种,故选A.
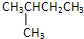 、
、 .
.若为CH3-CH2-CH2-CH2-CH3,相应烯烃有CH2═CH-CH2-CH2-CH3、CH3-CH═CH-CH2-CH3;CH2═CH-CH2-CH2-CH3氧化生成甲醛、丁醛,CH3-CH═CH-CH2-CH3氧化生成乙醛、丙醛;
若为
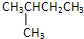 ,相应烯烃有:CH2═C(CH3)CH2CH3;CH3C(CH3)═CHCH3;CH3CH(CH3)CH═CH2;CH2═C(CH3)CH2CH3氧化可生成甲醛,CH3C(CH3)═CHCH3氧化生成乙醛,CH3CH(CH3)CH═CH2氧化可生成甲醛和2-甲基丙醛,
,相应烯烃有:CH2═C(CH3)CH2CH3;CH3C(CH3)═CHCH3;CH3CH(CH3)CH═CH2;CH2═C(CH3)CH2CH3氧化可生成甲醛,CH3C(CH3)═CHCH3氧化生成乙醛,CH3CH(CH3)CH═CH2氧化可生成甲醛和2-甲基丙醛,若为
 ,没有相应烯烃;
,没有相应烯烃;所以化学式为C5H10的烯烃在此条件下可生成醛的种类为5种,故选A.
点评:本题考查借助于信息考查了同分异构体的书写,难度中等,注意烯烃的同分异构体的书写方法,采取先写碳骨架异构、再移动C=C双键位置.

练习册系列答案
 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
下列各组物质,不用任何化学试剂,只需用相互反应的方法就能够鉴别的是( )
| A、盐酸、Na2CO3溶液、NaCl溶液、AgNO3溶液 |
| B、Cl2、HCl、HBr |
| C、BaCl2溶液、NaOH溶液、AgNO3溶液、NaCl溶液 |
| D、NaCl溶液、NaBr溶液、NaI溶液 |
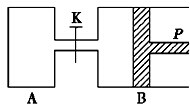 如图中,P为一可自由滑动的活塞,关闭K,分别向容器A、B中各充入2mol X、2mol Y,起始时,VA=a L,VB=0.8a L(连通管的体积忽略不计),在相同温度和有催化剂存在的条件下,两容器中各自发生下述反应:3X(g)+3Y(g)?2Z(g)+2W(g),达到平衡时,VB=0.6a L.下列说法错误的是( )
如图中,P为一可自由滑动的活塞,关闭K,分别向容器A、B中各充入2mol X、2mol Y,起始时,VA=a L,VB=0.8a L(连通管的体积忽略不计),在相同温度和有催化剂存在的条件下,两容器中各自发生下述反应:3X(g)+3Y(g)?2Z(g)+2W(g),达到平衡时,VB=0.6a L.下列说法错误的是( )| A、B中X的转化率为75% |
| B、A中X的转化率比B中的低 |
| C、平衡时A中混合气体密度比B小 |
| D、打开K,一段时间后反应再次达到平衡,则B的体积为1.2a L |
下列有关NH3的性质特点,描述错误的是( )
| A、极易溶于水,可与水做喷泉实验 |
| B、液氨能作制冷剂 |
| C、工业上常用氮气和氢气合成氨气 |
| D、常温下是无色无味气体,密度比空气小 |
下列变化中,由氧化反应引起的是( )
| A、乙烯通入酸性高锰酸钾溶液中,酸性高锰酸钾溶液褪色 |
| B、在一定条件下,苯与氢气反应生成环己烷 |
| C、在一定条件下,苯滴入浓硝酸和浓硫酸的混合液中,有油状物生成 |
| D、在催化剂作用下,乙烯分子间发生加成聚合反应生成高分子聚乙烯 |
实验室中分离水与植物油的混合液,必须使用的玻璃仪器是( )
A、 容量瓶 |
B、 集气瓶 |
C、 分液漏斗 |
D、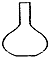 平地烧瓶 |
现有六种物质:铁粉、NaOH溶液、Ba(NO3)2溶液、稀硫酸、Fe2O3和CuSO4溶液,将它们两两混合后,能发生的化学反应共有( )
| A、7个 | B、6个 | C、5个 | D、4个 |
能证明硫元素的非金属性比氯元素弱的主要事实是( )
①氯气可溶于水而硫难溶于水
②硫最高价态为+6而氯最高价态为+7
③铁与氯气化合生成三氯化铁,铁与硫化合生成硫化亚铁
④将氯气通入硫化钠溶液,有淡黄色沉淀产生.
①氯气可溶于水而硫难溶于水
②硫最高价态为+6而氯最高价态为+7
③铁与氯气化合生成三氯化铁,铁与硫化合生成硫化亚铁
④将氯气通入硫化钠溶液,有淡黄色沉淀产生.
| A、①② | B、②③ | C、③④ | D、②④ |
已知N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ?mol-1,在温度相同、容积均为2L的3个恒容密闭容器中,按不同方式投入反应物,保持恒温,测得反应达到平衡时的有关数据如下,下列说法正确的是( )
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol N2、3mol H2 | 2mol N2、6mol H2 | 2mol NH3 |
| NH3的浓度(mol?L-1) | c1 | c2 | c3 |
| 反应的能量变化 | 放出Q1 kJ | 放出Q2 kJ | 吸收Q3 kJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | α1 | α2 | α3 |
| A、Q3+92.4c1=92.4 |
| B、α2+α3<1 |
| C、2p1=2p3<p2 |
| D、达到平衡时丙容器中NH3的体积分数最大 |