题目内容
【题目】人类最初使用的有机物大多源自于自然界,从樟科植物枝叶提取的精油中含有下列甲、乙、丙三种成分:

(1)甲中含氧官能团的名称为______,甲分子中处于同一平面的碳原子数量最多为___个。
(2)由甲转化为乙需经下列过程(己略去各步反应的无关产物,下同):

其中反应I的反应类型为______,反应Ⅱ的化学方程式为(注明反应条件)________。
(3)己知:RCHCHR![]() RCHO+RCHO;2HCHO
RCHO+RCHO;2HCHO![]() HCOOH+CH3OH
HCOOH+CH3OH
由乙制丙的一种合成路线图如下(A~F均为有机物,图中Mr表示相对分子质量):
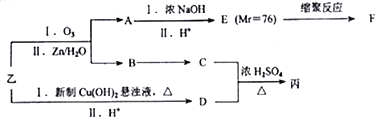
① 下列物质不能与C反应的是______(选填序号)
a.金属钠 b.HBr c.Na2CO3溶液 d.乙酸
②D有多种同分异构体,任写其中一种能同时满足下列条件的同分异构体结构简式_____。
a.苯环上连接着三种不同官能团 b.能发生银镜反应
c.能与Br2/CCl4发生加成反应 d.遇FeCl3溶液显示特征颜色
③ 写出乙与新制氢氧化铜悬浊液反应化学方程式________。
④ 写出F的结构简式_________。
⑥ 写出C和D反应生成丙的化学方程式__________。
【答案】 羟基 9 加成反应 ![]() c
c ![]()
![]()
![]()
![]()
【解析】(1)甲中含氧官能团是羟基,可以通过旋转连接苯环与C=C双键的C-C单键,使苯环与C=C双键构成的平面处于同一平面,分子中所以C原子都可能共面,故最多有9个C原子共面,故答案为:羟基;9;
(2)经过反应Ⅰ发现碳碳双键成为了单键,并且引入了Cl原子,所以反应为甲和氯化氢之间发生了加成反应,与氯原子相连的相邻碳原子含有氢原子,会发生消去反应生成乙,所以Ⅱ的方程式为:![]() +NaOH
+NaOH![]()
![]() +NaCl+H2O,故答案为:加成反应;
+NaCl+H2O,故答案为:加成反应;![]() +NaOH
+NaOH![]()
![]() +NaCl+H2O;
+NaCl+H2O;
(3)根据乙的结构简式和题干中所给信息,可知A是乙二醛,B是苯甲醛,乙在加热条件下与新制备氢氧化铜反应生成酸,D应为 ,则C应为醇,因B为苯甲醛,则C为苯甲醇,故丙为
,则C应为醇,因B为苯甲醛,则C为苯甲醇,故丙为![]() .E是相对分子质量为76,结合题给信息可知应为OH-CH2-COOH,本身能发生缩聚反应生成F为
.E是相对分子质量为76,结合题给信息可知应为OH-CH2-COOH,本身能发生缩聚反应生成F为![]() 。
。
①C为苯甲醇,含有羟基,可与钠反应生成氢气、与HBr发生取代反应、与乙酸发生酯化反应,不具有酸性,不能与碳酸钠反应,故答案为:c;
②该物质能发生银镜反应,一定含有醛基,可以和Br2/CCl4发生加成反应,含有碳碳碳双键,遇FeCl3溶液显示紫色,说明含有酚羟基,所以该物质的结构简式为![]() ,故答案为:
,故答案为:![]() ;
;
③乙为![]() ,含有醛基,可在加热条件下与新制备氢氧化铜浊液反应,方程式为C6H5CH=CHCHO+2Cu(OH)2+NaOH
,含有醛基,可在加热条件下与新制备氢氧化铜浊液反应,方程式为C6H5CH=CHCHO+2Cu(OH)2+NaOH![]() C6H5CH=CHCOONa+Cu2O↓+3H2O,故答案为:C6H5CH=CHCHO+2Cu(OH)2+NaOH
C6H5CH=CHCOONa+Cu2O↓+3H2O,故答案为:C6H5CH=CHCHO+2Cu(OH)2+NaOH![]() C6H5CH=CHCOONa+Cu2O↓+3H2O;
C6H5CH=CHCOONa+Cu2O↓+3H2O;
④由以上分析可知F为![]() ,故答案为:
,故答案为:![]() ;
;
⑤C和D反应生成丙的化学方程式为![]()
![]()
![]()
 ,故答案为:
,故答案为:![]() +
+![]()
![]()
 。
。

 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案【题目】铁及其化合物在工农业生产中有重要的作用。
(1)已知:C(s)+O2(g)=CO2(g) △H1=-393.5kJ/mol
②C(s)+CO2(g)=2CO(g) △H2=+172.5kJ/mol
③4Fe(s)+3O2(g)=2Fe2O3(g) △H3=-1651.0kJ/mol
CO还原氧化铁的热化学方程式为_______________________。
(2)高炉炼铁产生的高炉气中含有CO、H2、CO2等气体,利用CO和H2在催化剂作用下合成甲醇,是减少污染、节约能源的一种新举措,反应原理如下:CO(g)+2H2(g)=CH3OH(g) △H 。在体积不同的两个恒容密闭容器中分别充入1molCO和2moL H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如下图。

①在上图A、B、C三点中,选填下表物理且对应最大的点。
反应速率 | 平衡常数K | 平衡转化率a |
_________ | _________ | _________ |
②在300℃时,向C点平衡体系中再充入0.25molCO、0.5molH2和0.25mol的CH3OH,该反应向_________方向进行(城“正反应”、‘逆反应”或“不移动”)。
③一定温度下,CO的转化率与起始投料比[n(H2)/n(CO)]的变化关系如图所示,测得D点氢气的转化率为40%,则x=_____________。

(3)三氯化铁是一种重要的化合物,可以用来腐蚀电路板。某腐蚀废液中含有0.5mol·L-1Fe3+和0.26mol·L-1的Cu2+,欲使Fe3+完全沉淀[ c(Fe3+)≤4×l0-19]而Cu2+不沉淀,则需控制溶液pH的范围为_________。[KspCu(OH)2=2.6×l0-19;KspFe(OH)3=4×l0-38〕
(4)高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,工业上通过电解浓NaOH 溶液可制备Na2FeO4,然后转化为K2FeO4,电解原理如下图所示。

则A溶液中溶质的成分为___________________(填化学式);阳极的电极反应式为_____________



