��Ŀ����
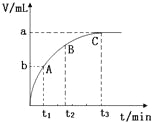
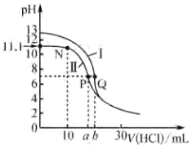
����Ŀ��25��ʱ����0.1000mol��L-1������ֱ�ζ�20.00mL 0.1000mol��L-1��ˮ��20.00mL 0.1000mol��L-1 NaOH��Һ���ζ�������ͼ��ʾ������˵������ȷ����
A.25����Kb(NH3��H2O)��������Ϊ10-5
B.N�㴦����Һ�У�c(NH![]() )>c(NH3��H2O)
)>c(NH3��H2O)
C.����II�ζ��յ�ʱ��ѡ��ָʾ��Ϊ��̪
D.Q��������������Ϊb mL����b=20
���𰸡�C
��������
����������������I��pH =13����Ϊ������Һ�ζ�NaOH��Һͼ������II������ζ���ˮ��Һͼ��
A. 25�����������pH =11.1�õ�![]() �����Kb(NH3��H2O)��������Ϊ105����A��ȷ��
�����Kb(NH3��H2O)��������Ϊ105����A��ȷ��
B. N�����ʵ�NH4Cl��NH3��H2O��Ũ����ȣ���Һ�Լ��ԣ�����ռ��Ҫ�������Һ�У�c(NH4+)��c(NH3��H2O)����B��ȷ��
C. ����II�ζ��յ�ʱ��Һ�����ԣ������ѡ��ָʾ��Ϊ���ȣ���C����
D. Q����NaOH��Һ��������еζ���������������Ϊb mL����Һ�����ԣ���b=20����D��ȷ��
������������ΪC��

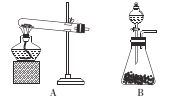
����Ŀ��������һ����Ҫ�Ĺ�ҵԭ�ϣ�Һ�ȴ��������е�˵�������£�
��װ | ��ƿ |
����Ҫ�� | Զ�������ĩ���������ࡢ�������ʣ�������������� |
й©���� | NaOH��NaHSO3��Һ���� |
���н�����ʵ�ķ���ʽ����ȷ����
A. ������������ˮ������Cl2 + H2O![]() 2H+ + Cl��+ ClO��
2H+ + Cl��+ ClO��
B. ��ⱥ��ʳ��ˮ��ȡCl2��2Cl�� +2H2O![]() 2OH��+ H2��+Cl2��
2OH��+ H2��+Cl2��
C. Ũ��ˮ����й¶���������������̣�8NH3 + 3Cl2 === 6 NH4Cl + N2
D. ������й©��������NaHSO3��Һ�����ã�HSO3��+ Cl2 + H2O === SO42��+ 3H+ + 2Cl��