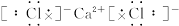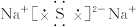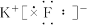题目内容
(8分)有X、Y、z、w四种短周期元素,原子序数依次增大,其核电荷数总和为38。Y元素原子最外层电子数占核外总电子数的3/4;W元素原子最外层电子数比同周期Z元素原子最外层电子数多5个电子;W和 Y不属于同一主族。
(1)画出Y原子结构示意图: ;
(2)从化合价角度分析,X元素可以排在周期表中I A、VIIA和 族;
(3)Z、W两种元素最高价氧化物对应水化合物相互反应的化学方程式: ;
(4)已知X2单质的热值为143 kJ·g-1,试写出X2单质在Y2单质中燃烧的热化学方程式: .
(1)画出Y原子结构示意图: ;
(2)从化合价角度分析,X元素可以排在周期表中I A、VIIA和 族;
(3)Z、W两种元素最高价氧化物对应水化合物相互反应的化学方程式: ;
(4)已知X2单质的热值为143 kJ·g-1,试写出X2单质在Y2单质中燃烧的热化学方程式: .
(8分)
(1)氧原子结构示产电图
(2)IVA (2分)
(2)Mg(OH)2+2HClO4=Mg(ClO4)2+2H2O(2分)
(4)H2(g)+1/2O2(g)=H2O(1); △H=-286kJ·mol-1(2分)
(1)氧原子结构示产电图

(2)IVA (2分)
(2)Mg(OH)2+2HClO4=Mg(ClO4)2+2H2O(2分)
(4)H2(g)+1/2O2(g)=H2O(1); △H=-286kJ·mol-1(2分)
考查原子核外电子的排布规律。Y元素原子最外层电子数占核外总电子数的3/4,由于最外层电子数最多是8个,所以Y的原子序数只能是8,即Y是氧元素。W元素原子最外层电子比同周期Z元素多5个电子,所以W的最外层电子数是6或7。又因为W和Y不属同一主族,所以W是第ⅦA的氯元素,则Z元素就是镁。四种元素的核电荷数是38,所以X是氢元素。
(1)氧原子结构示产电图
(2)H元素可呈+1价,排在IA族,可呈—1价,与VIIA族元素相似,正负价绝对值相同,与IVA族相当
(3)Mg(OH)2+2HClO4=Mg(ClO4)2+2H2O
(4)氢气的热值为143 kJ·g-1,可折算出2g氢气完全燃烧生成液态水时放出的热量为286kJ,则氢气燃烧的热化学方程式为:H2(g)+1/2O2(g)=H2O(1); △H=-286kJ·mol-1
(1)氧原子结构示产电图

(2)H元素可呈+1价,排在IA族,可呈—1价,与VIIA族元素相似,正负价绝对值相同,与IVA族相当
(3)Mg(OH)2+2HClO4=Mg(ClO4)2+2H2O
(4)氢气的热值为143 kJ·g-1,可折算出2g氢气完全燃烧生成液态水时放出的热量为286kJ,则氢气燃烧的热化学方程式为:H2(g)+1/2O2(g)=H2O(1); △H=-286kJ·mol-1

练习册系列答案
相关题目
 原子核外有49个电子
原子核外有49个电子