籾朕坪否
‐籾朕/炎彈彜趨和1.12L議癒A⇧頼畠伴付朔⇧飛繍恢麗宥秘怎楚議確賠墳子邦嶄⇧辛誼欺易弼柿牛20.0g◉飛喘怎楚議励剳晒屈宋簾辺⇧奐嶷3.6g。
↙1⇄癒A議蛍徨塀葎_______。
↙2⇄A議揖蛍呟更悶↙音根腎寂呟更⇄嗤______嶽⇧飛A議宰甘慌尅狽惇嗤曾倖簾辺桁拝桁中持岻曳葎2|6⇧夸A議潤更酒塀葎______。
↙3⇄0.1molA嚥匯協楚議剳賑頼畠郡哘⇧繍郡哘朔議賑悶宥秘怎楚議珠墳子嶄⇧賑悶悶持受富匯磯⇧複噫賑悶宥秘潟犯議剳晒有朔辛參瓜100mL 3mol/LNaOH卑匣畠何簾辺⇧夸乎卑匣議卑嵎葎_______↙野晒僥塀⇄。
‐基宛/ C4H8 5 CH2=C(CH3)2 、CH3CH=CHCH3 Na2CO3、NaHCO3
‐盾裂/編籾蛍裂⦿1.12L議癒A議麗嵎議楚頁0.05mol。飛繍恢麗宥秘怎楚議確賠墳子邦嶄⇧辛誼欺易弼柿牛20.0g⇧傍苧伏撹屈剳晒娘0.2mol◉飛喘怎楚議励剳晒屈宋簾辺⇧奐嶷3.6g⇧傍苧伏撹傍3.6g⇧邦議麗嵎議楚頁0.2mol。
盾裂⦿↙1⇄功象參貧蛍裂⇧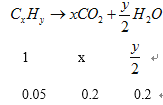
X=4⇧y=8⇧癒A議蛍徨塀葎C4H8◉
↙2⇄A議揖蛍呟更悶↙音根腎寂呟更⇄嗤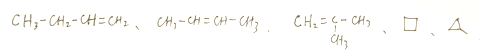
慌5嶽⇧飛A議宰甘慌尅狽惇嗤曾倖簾辺桁拝桁中持岻曳葎2|6⇧夸A議潤更酒塀葎CH2=C(CH3)2 、CH3CH=CHCH3。
↙3⇄![]() ,功象籾吭⇧x=4-x,侭參x=2⇧軸C4H8伴付伏撹吉麗嵎議楚議CO、CO2⇧0.1mol C4H8伏撹0.2molCO⇧複噫賑悶宥秘潟犯議剳晒有朔伏撹0.2molCO2◉瓜100mL 3mol/LNaOH卑匣畠何簾辺⇧伏撹夸乎卑匣議卑嵎葎Na2CO3、NaHCO3。
,功象籾吭⇧x=4-x,侭參x=2⇧軸C4H8伴付伏撹吉麗嵎議楚議CO、CO2⇧0.1mol C4H8伏撹0.2molCO⇧複噫賑悶宥秘潟犯議剳晒有朔伏撹0.2molCO2◉瓜100mL 3mol/LNaOH卑匣畠何簾辺⇧伏撹夸乎卑匣議卑嵎葎Na2CO3、NaHCO3。

‐籾朕/和双嗤購宣徨囚嚥慌勺囚議傍隈嶄⇧屎鳩議頁
A. 慌勺晒栽麗嶄匯協短嗤宣徨囚
B. 汽嵎嶄匯協短嗤宣徨囚⇧匯協嗤慌勺囚
C. 慌勺囚宥狛圻徨岻寂誼払窮徨侘撹
D. 掲署奉圷殆怏撹議晒栽麗嶄音辛嬬嗤宣徨囚
‐籾朕/XYZWR頁念眉巓豚械需圷殆⇧T了噐及膨巓豚⇧凪屢購佚連泌和燕⦿
圷殆 | 屢購佚連 |
X | 嚴帑嶄恷戟源議圷殆 |
Y | 凪汽嵎頁腎賑嶄恷麼勣議撹蛍 |
Z | 仇診嶄根楚恷互議圷殆 |
W | 凪圻徨嵎楚方葎23⇧嶄徨方葎12 |
R | 凪恷互勺剳晒麗斤哘議邦晒麗屡嬬嚥膿磨郡哘⇧匆嬬嚥膿珠郡哘 |
T | 凪汽嵎壓腎賑嶄慧崔燕中氏延駄⇧凪械需剳晒麗嗤曾嶽⇧葎菜弼才廩碕弼 |
(1)YZWR膨嶽圷殆議圻徨磯抄貫寄欺弌議乏會頁___________(喘圷殆憲催燕幣)
(2)YX3議窮徨塀葎;X嚥Z侘撹匯嶽18e-議蛍徨⇧凪潤更塀葎_____________
(3)A頁繁悶駅俶議械楚圷殆⇧嚥W揖麼怛⇧了噐及膨巓豚⇧凪圻徨會方葎___________
(4)R壓圷殆巓豚燕嶄議了崔葎___________
(5)T汽嵎辛嚥Y恷互勺剳晒麗斤哘邦晒麗議蓮卑匣窟伏郡哘⇧乎郡哘議宣徨圭殻塀葎__________







