题目内容
某温度下,容积一定的密闭容器中进行如下可逆反应:
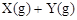
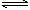
 ;
;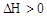 ,下列叙述正确的是( )
,下列叙述正确的是( )
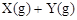
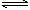
 ;
;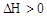 ,下列叙述正确的是( )
,下列叙述正确的是( )| A.加入少量W,逆反应速率增大 |
B.平衡后加入X,上述反应的 增大 增大 |
| C.升高温度,平衡逆向移动 |
| D.混合气体密度不变,不能作为反应达到平衡的标志 |
B
A 错,加入固体,不影响反应速率
B 对加入X,平衡右移, 增大
增大
C 错升温,平衡向吸热的方向移动,即正向移动
D 错密度="m/v" 在反应未平衡时,气体质量是变量,所以可用密度做平衡的标志
B 对加入X,平衡右移,
 增大
增大C 错升温,平衡向吸热的方向移动,即正向移动
D 错密度="m/v" 在反应未平衡时,气体质量是变量,所以可用密度做平衡的标志

练习册系列答案
相关题目
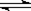 4 C(g) 2min时反应达到平衡状态(温度不变),并测得C 的浓度为0.4 mol/L,请填写下列空白:
4 C(g) 2min时反应达到平衡状态(温度不变),并测得C 的浓度为0.4 mol/L,请填写下列空白: 2Z(g)(正反应为放热反应),为了使平衡向生成Z的方向移动,应选择下列的适宜条件是( )
2Z(g)(正反应为放热反应),为了使平衡向生成Z的方向移动,应选择下列的适宜条件是( ) 4C(g)+D(g)反应10min后达平衡,此时D的浓度为0.5mol/L。下列说法正确的是
4C(g)+D(g)反应10min后达平衡,此时D的浓度为0.5mol/L。下列说法正确的是  A的转化率一定大于50%
A的转化率一定大于50%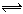 2AB2(g) 达到平衡状态的标志是 ( )
2AB2(g) 达到平衡状态的标志是 ( )
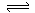 2C0(g) △H>O,K1 ①
2C0(g) △H>O,K1 ①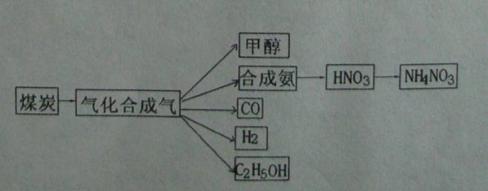


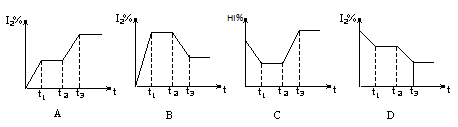
 H2(g)+I2(g);△H>0,在t1时达到平衡,t2时加热升温并保温,到t3时又达到新平衡,符合这一变化的图像是 ( )
H2(g)+I2(g);△H>0,在t1时达到平衡,t2时加热升温并保温,到t3时又达到新平衡,符合这一变化的图像是 ( )