��Ŀ����
����Ŀ������������ҽҩ��ҵ�����ںϳ�ͷ������������ƥĪ�ֵȵ��м��壬����·���Ǻϳɿ������ἰ���������һ�ַ�����

(1)��д��B�Ľṹ��ʽ_____��C�й����ŵ�����Ϊ_____��
(2)��Ӧ�ٵķ�Ӧ����Ϊ_____��D�ĺ˴Ź���������_____��塣
(3)1molE��������_____molNaOH��Ӧ����Ӧ�۵Ļ�ѧ����ʽΪ_____��
(4)����C���ӿ��Է�Ӧ���ɾ���������Ԫ���Ļ�����F����F�Ľṹ��ʽΪ_____��
(5)д����������������C��ͬ���칹��Ľṹ��ʽ_____��
A�����ܷ���������Ӧ�����ܷ���ˮ�ⷴӦ
B����FeCl3������ɫ
C�������Ͼ�������λ�ڶ�λ��ȡ����
(6)��֪��RCH2COOH![]() RCHClCOOH�����Ա�����Ϊԭ�ϣ����Լ���ѡ������Ʊ����Ҵ��ᣨ
RCHClCOOH�����Ա�����Ϊԭ�ϣ����Լ���ѡ������Ʊ����Ҵ��ᣨ![]() ���ĺϳ�·��_____��
���ĺϳ�·��_____��
���𰸡�OHCCOOH �ǻ����Ȼ� �ӳɷ�Ӧ 6 2 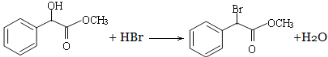
![]()
![]()
��������
��1����A�ķ���ʽ��֪AΪ![]() ������A��B��C�ķ���ʽ��֪A+B��CӦΪ�ӳɷ�Ӧ������C��A�Ľṹ��ʽ��B�ķ���ʽ������֪BΪ
������A��B��C�ķ���ʽ��֪A+B��CӦΪ�ӳɷ�Ӧ������C��A�Ľṹ��ʽ��B�ķ���ʽ������֪BΪ![]() ��
��
��2�����D�Ľṹ���õ�Ч�ⷨ�����˴Ź���������������
��3��E�Ľṹ�к�����������ԭ�����ֹ����ţ���Ӧ��Ϊ�ǻ����������ȡ����Ӧ��
��4������C���ӷ���������Ӧ�����������ݴ˷�����ṹ��ʽ��
��5��A�����ܷ���������Ӧ�����ܷ���ˮ�ⷴӦ��˵������ȩ����������B����FeCl3������ɫ��˵�������ǻ����ٽ�Ϲ����ŵ�λ��Ϊ��λ����������
��6����ϸ�����Ϣ��������ϳɷ���������������
��1��A+B��C��Ϊ��������B�ļӳɷ�Ӧ���������Ʒ����Ƴ�B�Ľṹ��ʽΪOHCCOOH�������֪��C�Ľṹ��ʽ�ɿ�����C�к��еĹ�����Ϊ�ǻ����Ȼ���
�ʴ�Ϊ��OHCCOOH���ǻ����Ȼ���
��2��������������֪��Ӧ��Ϊ�ӳɷ�Ӧ�����ݵ�Ч�ⷨ��֪��D��6�ֲ�ͬ��������ԭ�ӣ��˴Ź���������6��壬
��Ϊ���ӳɷ�Ӧ��6��
��3����E�Ľṹ�к�����������ԭ�����ֹ����ţ�1 mol������1 mol�������Ʒ���ˮ�ⷴӦ��1 mol��ԭ��Ҳ����1 mol ��������ˮ��Һ����ˮ�ⷴӦ����1molE��������2 molNaOH��Ӧ����Ӧ��Ϊ�ǻ����������ȡ����Ӧ�����仯ѧ����ʽΪ�� 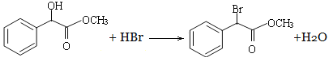 ��
��
�ʴ�Ϊ��2��  ��
��
��4��C����Ϊ �������ں��Ȼ��봼�ǻ�������������֪������C���ӷ���������Ӧ�������������仯ѧ����ʽΪ��
�������ں��Ȼ��봼�ǻ�������������֪������C���ӷ���������Ӧ�������������仯ѧ����ʽΪ�� 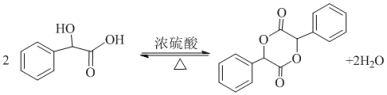 ����FΪ
����FΪ
�ʴ�Ϊ�� ��
��
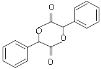
��5����������������֪��C��ͬ���칹���м��ܷ���������Ӧ�����ܷ���ˮ�ⷴӦ��Ҫ����ȩ��������������Ϊ�����������FeCl3������ɫ�����京���ǻ��������Ͼ�������λ�ڶ�λ��ȡ�����������ͬ���칹��Ϊ![]() ��
��
��6���ɱ�����ϳ�![]() ������ṹ��֪�ø߷���Ϊ������������ϳɷ���������һ������Ϊ
������ṹ��֪�ø߷���Ϊ������������ϳɷ���������һ������Ϊ![]() ,������֪����������һ������Ϊ
,������֪����������һ������Ϊ![]() ������CH3COOHת����������˺ϳ�·��Ϊ
������CH3COOHת����������˺ϳ�·��Ϊ![]() ��
��

����Ŀ��ijұ�������ú�ZnO���̻��ѳ���ҵ�����е�SO2�����յõ�п�Ρ��ó������̻ҵ���Ҫ�ɷ����±���ʾ��
��Ҫ�ɷ� | ZnO | CaO | Fe2O3 | SiO2 | ���� |
��������/% | 81 | 0.098 | 1.14 | 0.5 | �������� |
��һ�������£�����SO2�Ĺ�ҵ����ͨ���̻ҽ�Һ(�̻Һ�ˮ�Ļ����)�����������в��pH������Һ���ܽ��SO2���ʵ���Ũ��[c(SO2)]��ʱ��ı仯��ͼ��ʾ��

(1)��ZnO��Һ��pHΪ6.8���������̻ҽ�Һ�ij�ʼpHΪ7.2���ڿ�ʼ�����3 min��(a~b��)��pHѸ�ٽ���6.8������pHѸ�ٱ仯��ԭ����_____(��ϻ�ѧ�������)��
(2)�������ѳ�SO2Ч����ѵ�ʱ�䷶Χ��_____(����ĸ���)��
A��20~30 min B��30~40 min C��50~60 min D��70~80 min
(3)������������漰������Ҫ��Ӧԭ����
����ZnO + SO2 === ZnSO3��
����ZnSO3 + SO2 + H2O === Zn(HSO3)2
����30~40 minʱ����Ҫ������ӦII�����ɿ����Ե�Zn(HSO3)2������Һ��c(SO2)������ԭ�������______��
����30~80 minʱ��pH���͵�ԭ�������______(д��2��)��
�۽������Ļ�������ÿ������������������ù����з�����Ӧ��2ZnSO3 + O2 === 2ZnSO4��______��
����Ŀ�������£���0.1mol/L������������Һ��0.06mol/L������Һ�������ϣ���Һ��pH����
A. 1.7 B. 2.0 C. 10 D. 12
����Ŀ���±��г��ĶԾ����˵���У�������ǣ� ��
ѡ�� | A | B | C | D |
�������� | �⻯�� | �ɱ� | �������� | �� |
�����е����� | ���������� | ���� | ԭ�� | ���� |
���Ӽ������ | ���Ӽ� | ���Ӽ�������� | ���ۼ� | ���ۼ� |
A.AB.BC.CD.D


