题目内容
1.下列现象或操作不适宜用勒夏特列原理解释的是( )| A. | 实验室可用CaO和浓氨水快速制取氨气 | |
| B. | FeCl3溶液中加Fe粉,颜色由棕黄色变为浅绿色 | |
| C. | 新制氯水放置一段时间颜色变浅 | |
| D. | 工业上在高压条件下制取氨气 |
分析 勒夏特列原理为:如果改变影响平衡的条件之一,平衡将向着能够减弱这种改变的方向移动.使用勒夏特列原理时,该反应必须是可逆反应,否则勒夏特列原理不适用.
解答 解:A.浓氨水加入CaO固体,CaO固体溶于水生成氢氧化钙,该反应放热,化学平衡NH3+H2O?NH3•H2O?NH4++OH-逆向进行,有利于氨气生成,能用化学平衡移动原理解释,故A不选;
B.铁离子与铁的反应生成亚铁离子,该反应不是可逆反应,不能用勒夏特列原理解释,故B选;
C.氯水中存在氯气与水的反应平衡,反应生成的次氯酸容易分解,导致氯气与水的反应向着正向移动,最终氯气完全反应,溶液颜色消失,该变化与平衡移动有关,能用化学平衡移动原理解释,故C不选;
D.合成氨反应为N2+3H2?2NH3,增大压强平衡向正方向移动,可用勒夏特列原理解释,故D不选;
故选B.
点评 本题考查勒夏特列原理,题目难度不大,明确勒夏特列原理的内容为解答关键,注意使用勒夏特列原理的前提必须是可逆反应,且是否发生平衡的移动.

练习册系列答案
相关题目
11.在一密闭容器中盛有aLCl2和H2的混合气体,用电火花引燃后,恢复到原来状态,发现气体仍为aL.用足量的NaOH溶液吸收燃烧后的气体,结果无气剩余.由以上条件,推知原混合气体中Cl2和H2物质的量之比一定是
( )
( )
| A. | Cl2:H2=1 | B. | Cl2:H2<1 | C. | Cl2:H2≥1 | D. | Cl2:H2>1 |
12.化学与生产生活密切相关,下列有关说法不正确的是( )
| A. | 大量使用含磷洗衣粉会造成生活污水的富营养化 | |
| B. | 用未经处理的电镀厂废水灌溉农田,易造成土壤重金属污染 | |
| C. | 臭氧一生物活性炭用于自来水深度处理,利用了活性炭的还原性 | |
| D. | 纳米铁粉可将地下水中的NO3-转化为N2,是因为纳米铁具有还原性 |
9.下列化学反应在冶金工业中没有得到广泛应用的是( )
| A. | MgCl2(熔融)$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑ | B. | Al2O3+3C$\frac{\underline{\;高温\;}}{\;}$2Al+3CO↑ | ||
| C. | Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | D. | 2Ag2O$\frac{\underline{\;\;△\;\;}}{\;}$4Ag+O2↑ |
16.如图是SO2(g)和O2(g)的能量变化示意图,由图可知( )


| A. | 2SO2(g)+O2 (g)?2SO3 (g)-197.8kJ | B. | 2SO2 (g)+O2 (g)?2SO3 (g)+197.8kJ | ||
| C. | 2SO2 (g)+O2 (g)?2SO3 (g)+98.9kJ | D. | 2SO2 (g)+O2 (g)?2SO3 (g)-98.9kJ |
6.下列比较错误的是( )
| A. | 稳定性:CH4>SiH4 | B. | 碱性:Mg(OH )2>Ca(OH )2 | ||
| C. | 羟基中H的活泼性:H2O>CH3CH2OH | D. | 原子半径:S>Cl |
13.下列说法中正确的是( )
| A. | 每一周期的元素都是从碱金属开始,最后以稀有气体结束 | |
| B. | 同一周期中(除第一周期外),从左到右,各元素原子核的电子数都是从1个逐渐增加到8个 | |
| C. | 元素周期表一共有7个周期,16个族 | |
| D. | 第七周期只有23种元素 |
10.一种熔融碳酸盐燃料电池原理示意如图.下列有关该电池的说法正确的是( )
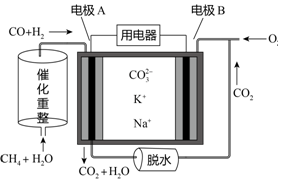

| A. | 电极A上H2和CO都发生了氧化反应 | |
| B. | 反应CH4+H2O$\frac{\underline{\;催化剂\;}}{△}$3H2+CO,每消耗1molCH4转移12mol电子 | |
| C. | 电池工作时,电能转变为化学能 | |
| D. | 电极B上发生的电极反应为:O2+2H2O+4e-═4OH- |
11.下列物质属于电解质的是( )
| A. | Cu | B. | NaCl溶液 | C. | KNO3 | D. | C2H5OH |