题目内容
下列离子方程式正确的是( )
| A、用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2O |
| B、醋酸钠溶液和盐酸混合:CH3COONa+H+=CH3COOH+Na+ |
| C、氢氧化钡溶液与稀硫酸反应:Ba2++SO42-+H++OH-=BaSO4↓+H2O |
| D、少量金属钠放入冷水中:Na+2H2O=Na++2OH-+H2↑ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.碳酸氢钠和稀盐酸反应生成二氧化碳、水和氯化钠;
B.强电解质写离子;
C.二者反应生成硫酸钡和水的物质的量之比为1:2;
D.电荷不守恒.
B.强电解质写离子;
C.二者反应生成硫酸钡和水的物质的量之比为1:2;
D.电荷不守恒.
解答:
解:A.碳酸氢钠和稀盐酸反应生成二氧化碳、水和氯化钠,离子方程式为HCO3-+H+=CO2↑+H2O,故A正确;
B.强电解质写离子,离子方程式为CH3COO-+H+=CH3COOH,故B错误;
C.二者反应生成硫酸钡和水的物质的量之比为1:2,离子方程式为Ba2++SO42-+2H++2OH-=BaSO4↓+2H2O,故C错误;
D.电荷不守恒,离子方程式为2Na+2H2O=2Na++2OH-+H2↑,故D错误;
故选A.
B.强电解质写离子,离子方程式为CH3COO-+H+=CH3COOH,故B错误;
C.二者反应生成硫酸钡和水的物质的量之比为1:2,离子方程式为Ba2++SO42-+2H++2OH-=BaSO4↓+2H2O,故C错误;
D.电荷不守恒,离子方程式为2Na+2H2O=2Na++2OH-+H2↑,故D错误;
故选A.
点评:本题考查了离子方程式正误判断,明确物质之间的反应再结合离子方程式书写规则分析即可,注意要遵循客观事实、原子守恒、电荷守恒及转移电子守恒,易错选项是C.

练习册系列答案
相关题目
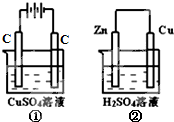 如图两个装置中,液体体积均为200mL,开始工作前电解质溶液的浓度均为0.5mol/L,工作一段时间后,测得有0.02mol电子通过,若忽略溶液体积的变化.下列叙述正确的是( )
如图两个装置中,液体体积均为200mL,开始工作前电解质溶液的浓度均为0.5mol/L,工作一段时间后,测得有0.02mol电子通过,若忽略溶液体积的变化.下列叙述正确的是( )| A、产生气体体积:①=② |
| B、溶液的pH变化:①②均减小 |
| C、电极反应式:①中阳极为4OH--4e-═2H2O+O2↑,②中负极为2H++2e-═H2↑ |
| D、①中阴极质量增加,②中正极质量不变 |
把a L硫酸铵和硝酸铵混合液分成两等份,一份需用b mol烧碱刚好把氨全部赶出,另一份与BaCl2溶液反应恰好消耗c mol BaCl2.原则溶液中NO3-的物质的量浓度是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列各组离子中,在碱性溶液中能大量共存,且溶液为无色透明的是( )
| A、K+、MnO4-、SO42-、Cl- |
| B、Ca2+、HCO3-、NO3-、SO42- |
| C、K+、NO3-、SO42-、CO32- |
| D、Mg2+、SO42-、CO32-、Cl- |
 由化学能转变的热能或电能仍然是人类使用的主要能源.根据图所示的装置,判断下列说法不正确的是( )
由化学能转变的热能或电能仍然是人类使用的主要能源.根据图所示的装置,判断下列说法不正确的是( )| A、该装置中Pt极为阳极 |
| B、当c极的质量变化了2.16g时,a极上消耗的O2的体积为1.12L |
| C、该装置中b极的电极反应式是:H2+2OH--2e-═2H2O |
| D、该装置中a极为正极,发生还原反应 |
实验室用密度为1.84g/cm3 98%的浓硫酸与密度为1.1g/cm3 15%的稀硫酸混合配制密度为1.4g/cm3 59%的硫酸溶液,取浓、稀硫酸的体积比最接近的值是( )
| A、1:2 | B、2:1 |
| C、3:2 | D、2:3 |
下列关于乙醇的说法正确的是( )
| A、常温下是一种无色无味的液体 |
| B、能和乙酸发生加成反应 |
| C、能和Na2CO3溶液反应 |
| D、可发生氧化反应 |
 【化学-选修5:有机化学基础】
【化学-选修5:有机化学基础】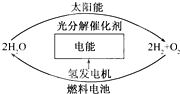 《全球科技经济瞭望》报道了美国氢燃料电池技术的发展.科学家预测“氢能”将是未来21世纪最理想的新能源,氢能是利用氢气的燃烧反应放热提供能量.
《全球科技经济瞭望》报道了美国氢燃料电池技术的发展.科学家预测“氢能”将是未来21世纪最理想的新能源,氢能是利用氢气的燃烧反应放热提供能量.