题目内容
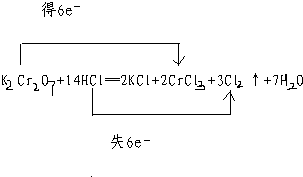
在K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O反应中,
Cl
Cl
元素被氧化,K2Cr2O7
K2Cr2O7
是氧化剂,还原产物是CrCl3
CrCl3
,电子转移的数目是6
6
.分析:化合价升高的元素被氧化,化合价降低的元素所在的反应物是氧化剂,对应的产物是还原产物,化合价升高的元素所在的反应物是还原剂,化合价升高数目=化合价降低数目=转移的电子数目.
解答:解:在K2Cr2O7+14HCl═2KCl+2CrCl3+3Cl2↑+7H2O反应中,氯元素化合价升高,所以氯元素被氧化,铬元素化合价降低,所以K2Cr2O7是氧化剂,对应的产物CrCl3是还原产物,化合价升高数目=化合价降低数目=转移的电子数目=6.
故答案为:Cl;K2Cr2O7;CrCl3;6.
故答案为:Cl;K2Cr2O7;CrCl3;6.
点评:本题考查氧化还原反应中的有关概念和电子转移知识,可以根据所学知识进行回答,较简单.

练习册系列答案
相关题目