题目内容
(10分)m、n、x、y四种主族元素在周期表的相对位置如下图所示。已知它们的原子序数总和为46,则:
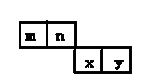
(1)元素n的气态氢化物的分子式为 ,空间构型为 ,n原子的价电子排布式是_______
(2)m与y所形成的化合物含 键,属 分子。(填“极性”或“非极性”)
(3)x位于周期表的第 周期第 族;其简单离子的离子结构示意图为 。
(4)由n、y的氢化物相互作用所生成的物质的电子式为 。

(1)元素n的气态氢化物的分子式为 ,空间构型为 ,n原子的价电子排布式是_______
(2)m与y所形成的化合物含 键,属 分子。(填“极性”或“非极性”)
(3)x位于周期表的第 周期第 族;其简单离子的离子结构示意图为 。
(4)由n、y的氢化物相互作用所生成的物质的电子式为 。
(10分)⑴NH3, (1分) 三角锥型,(1分) ,2s22p3 (1分)
⑵极性、(1分) 非极性(1分) ⑶三,(1分) VIA, (1分) (1分)
(1分)
⑷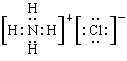 (2分),
(2分),
⑵极性、(1分) 非极性(1分) ⑶三,(1分) VIA, (1分)
 (1分)
(1分)⑷
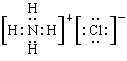 (2分),
(2分),设m元素的原子序数是a,则n就是a+1,x就是a+10,y就是a+11,所以a+a+1+a+10+a+11=46,解得a=6,所以m、n、x、y四种主族元素分别是C、N、S、Cl。
(1)氮元素的氢化物是氨气,化学式是NH3;空间构形是三角锥形;根据构造原理可知,n原子的价电子排布式是2s22p3。
(2)C与Cl都是非金属,形成化合物是四氯化碳,属于正四面体形结构,所以是含有极性键的非极性分子。
(3)S的原子序数是16,位于第三正确VIA,硫离子的原子核外电子数是18个,因此离子的结构示意图是 。
。
(4)氨气与氯化氢形成的化合物是氯化铵,属于离子化合物,电子式是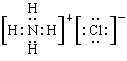 。
。
(1)氮元素的氢化物是氨气,化学式是NH3;空间构形是三角锥形;根据构造原理可知,n原子的价电子排布式是2s22p3。
(2)C与Cl都是非金属,形成化合物是四氯化碳,属于正四面体形结构,所以是含有极性键的非极性分子。
(3)S的原子序数是16,位于第三正确VIA,硫离子的原子核外电子数是18个,因此离子的结构示意图是
 。
。(4)氨气与氯化氢形成的化合物是氯化铵,属于离子化合物,电子式是
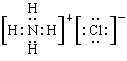 。
。
练习册系列答案
相关题目