题目内容
【题目】课外实践活动中取某地石灰石样品12g进行探究实验,现将100g稀盐酸分五次加入石灰石样品中(杂质不溶于水也不参与反应),充分反应后测得生成气体的总质量如下表所示:
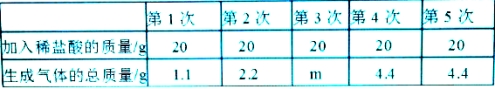
试求:(1)m的值为
(2)12g石灰石样品中碳酸钙的质量
(3)反应完全后最终溶液中氯化钙的质量分数?
【答案】(1)3.3
(2)解:设石灰石样品中碳酸钙的质量为x,反应完全后最终溶液中氯化钙的质量为y
CaCO3+2HCl=CaCl2+H20+CO2↓
100 111 44
X y 4.4g
![]() =
=![]()
![]() =
=![]()
X =10g y=11.1g
(3)![]() ×100%≈10.5%
×100%≈10.5%
答:石灰石样品中碳酸钙的质量为10g,反应完全后最终溶液中氯化钙的质量为10.5%。
【解析】
试题分析:(1)根据记录数据可发现,20g的盐酸完全反应生成二氧化碳气体的质量是1.1g,第4次实验中加入盐酸生成的二氧化碳是4.4g,说明了第三次实验中盐酸完全反应,可推出m的值为3.3g。
故答案为:3.3;
(2)设石灰石中CaCO3的质量为x,生成的氯化钙的质量为y.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 111 44
x y 4.4g
![]()
解得:x=10g y=11.1g。
故答案为:10g;
(3)完全反应后最终溶液中氯化钙的质量分数是:![]() ×100%≈10.5%
×100%≈10.5%
故答案为:10.5%。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目