题目内容
(2012?延边州模拟)某链状烃A的蒸汽密度是相同条件下氧气的2.625倍,在一定条件下1mol A与1molHCl加成只能得到Q1,1mol A与1molH2加成可以得到烷烃P,P在光照条件下与氯气发生取代反应,只得到两种一氯代烃Q1和Q2.
(1)A的分子式为
(2)Q1的结构简式为
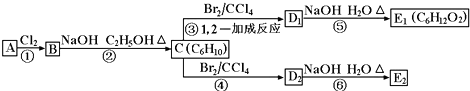
(3)在如图中,D1、D2互为同分异构体,E1、E2互为同分异构体,反应②的化学方程式为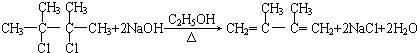
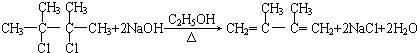 .
.
(4)E1的同分异构体很多,其中属于酯类、核磁共振氢谱中只有两种氢的同分异构体有
(5)E2的结构简式是
 ;④的反应类型是
;④的反应类型是

(1)A的分子式为
C6H12
C6H12
;(2)Q1的结构简式为
(CH3)2CClCH(CH3)2
(CH3)2CClCH(CH3)2
;(3)在如图中,D1、D2互为同分异构体,E1、E2互为同分异构体,反应②的化学方程式为
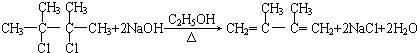
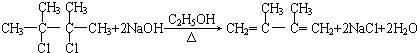
(4)E1的同分异构体很多,其中属于酯类、核磁共振氢谱中只有两种氢的同分异构体有
2
2
种,写出其中一种的结构简式(CH3)3CCOOCH3或CH3COOC(CH3)3
(CH3)3CCOOCH3或CH3COOC(CH3)3
.(5)E2的结构简式是


加成反应
加成反应
.分析:某链状烃A的蒸汽密度是相同条件下氧气的2.625倍,则其相对分子质量为2.625×32=84,烃分子中C原子最大数目=
=7,故A分子式为C6H12,分子中含有1个C=C双键,1mol A与1molHCl加成只能得到Q1,1mol A与1molH2加成可以得到烷烃P,P在光照条件下与氯气发生取代反应,只得到两种一氯代烃Q1和Q2,则A为对称结构,且与氢气加成后的产物含有2种H原子,则A分子中C=C双键不饱和碳原子连接2个甲基,则A为(CH3)2C=C(CH3)2,故Q1为(CH3)2CClCH(CH3)2,Q1为(CH3)2CHCH(CH3)CH2Cl.顺推可得,B为(CH3)2CClCCl(CH3)2,C为H2C=C(CH3)C(CH3)=CH2,C与溴发生1,2-加成反应生成D1为BrCH2CBr(CH3)C(CH3)=CH2,在氢氧化钠水溶液、加热条件下发生水解反应生成E1为HOCH2C(OH)(CH3)C(CH3)=CH2.C与溴发生1,4-加成生成D2为BrCH2C(CH3)=C(CH3)CH2Br,在氢氧化钠水溶液、加热条件下发生水解反应生成E2为HOCH2C(CH3)=C(CH3)CH2OH,据此电解.
| 84 |
| 12 |
解答:解:某链状烃A的蒸汽密度是相同条件下氧气的2.625倍,则其相对分子质量为2.625×32=84,烃分子中C原子最大数目=
=7,故A分子式为C6H12,分子中含有1个C=C双键,1mol A与1molHCl加成只能得到Q1,1mol A与1molH2加成可以得到烷烃P,P在光照条件下与氯气发生取代反应,只得到两种一氯代烃Q1和Q2,则A为对称结构,且与氢气加成后的产物含有2种H原子,则A分子中C=C双键不饱和碳原子连接2个甲基,则A为(CH3)2C=C(CH3)2,故Q1为(CH3)2CClCH(CH3)2,Q1为(CH3)2CHCH(CH3)CH2Cl.顺推可得,B为(CH3)2CClCCl(CH3)2,C为H2C=C(CH3)C(CH3)=CH2,C与溴发生1,2-加成反应生成D1为BrCH2CBr(CH3)C(CH3)=CH2,在氢氧化钠水溶液、加热条件下发生水解反应生成E1为HOCH2C(OH)(CH3)C(CH3)=CH2.C与溴发生1,4-加成生成D2为BrCH2C(CH3)=C(CH3)CH2Br,在氢氧化钠水溶液、加热条件下发生水解反应生成E2为HOCH2C(CH3)=C(CH3)CH2OH,
(1)由上述分析可知,A的分子式为C6H12,故答案为:C6H12;
(2)由上述分析可知,Q1的结构简式为(CH3)2CClCH(CH3)2,故答案为:(CH3)2CClCH(CH3)2;
(3)反应②的化学方程式为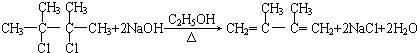 ,
,
故答案为: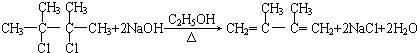 ;
;
(4)E1为HOCH2C(OH)(CH3)C(CH3)=CH2,其属于酯类、核磁共振氢谱中只有两种氢的同分异构体,
同分异构体中含有1个酯基,形成酯的羧酸、醇分子中含有2种H原子,符号条件同分异构体为(CH3)3CCOOCH3、CH3COOC(CH3)3,
故答案为:2;(CH3)3CCOOCH3或CH3COOC(CH3)3;
(5)E2的结构简式是 ;反应④属于加成反应,
;反应④属于加成反应,
故答案为: ;加成反应.
;加成反应.
| 84 |
| 12 |
(1)由上述分析可知,A的分子式为C6H12,故答案为:C6H12;
(2)由上述分析可知,Q1的结构简式为(CH3)2CClCH(CH3)2,故答案为:(CH3)2CClCH(CH3)2;
(3)反应②的化学方程式为
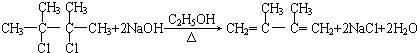 ,
,故答案为:
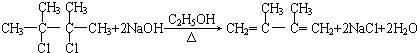 ;
;(4)E1为HOCH2C(OH)(CH3)C(CH3)=CH2,其属于酯类、核磁共振氢谱中只有两种氢的同分异构体,
同分异构体中含有1个酯基,形成酯的羧酸、醇分子中含有2种H原子,符号条件同分异构体为(CH3)3CCOOCH3、CH3COOC(CH3)3,
故答案为:2;(CH3)3CCOOCH3或CH3COOC(CH3)3;
(5)E2的结构简式是
 ;反应④属于加成反应,
;反应④属于加成反应,故答案为:
 ;加成反应.
;加成反应.点评:本题考查有机物的推断,涉及烯烃与卤代烃性质、同分异构体书写、有机反应类型等,难度中等,根据信息确定烃A的结构是关键,对学生的逻辑推理有一定的要求.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目