题目内容
【题目】二甲醚又称甲醚,简称DME,熔点-141.5 ℃,沸点-24.9 ℃,与石油液化气(LPG)相似,被誉为“21世纪的清洁燃料”。制备原理如下:
Ⅰ.由天然气催化制备二甲醚:
①2CH4(g)+O2(g)![]() CH3OCH3(g)+H2O(g) H1
CH3OCH3(g)+H2O(g) H1
Ⅱ.由合成气制备二甲醚:
②CO(g)+2H2(g)![]() CH3OH(g) H2=-90.7 kJ·mol-1
CH3OH(g) H2=-90.7 kJ·mol-1
③2CH3OH(g)![]() CH3OCH3(g)+H2O(g) H3
CH3OCH3(g)+H2O(g) H3
回答下列问题:
(1)若甲烷和二甲醚的燃烧热分别是890.3 kJ·mol-1、1453.0 kJ·mol-1;1mol液态水变为气态水要吸收44.0 kJ的热量。反应③中的相关的化学键键能数据如下:
化学键 | H-H | C-O | H-O(水) | H-O(醇) | C-H |
E/(kJ.mol-1) | 436 | 343 | 465 | 453 | 413 |
则H1=__________kJ·mol-1、H3=__________kJ·mol-1
(2)反应①的化学平衡常数表达式为_____________。
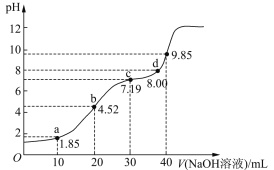
制备原理Ⅰ中,在恒温、恒容的密闭容器中合成,将气体按n(CH4):n(O2)=2:1混合,能正确反映反应①中CH4的体积分数随温度变化的曲线是_______________。

下列能表明反应①达到化学平衡状态的是________。
a.混合气体的密度不变
b.反应容器中二甲醚的百分含量不变
c.反应物的反应速率与生成物的反应速率之比等于化学计量数之比
d.混合气体的压强不变
(3)有人模拟制备原理Ⅱ,在500K时的2L的密闭容器中充入2molCO和6molH2,8min达到平衡,平衡使CO的转化率为80%,c(CH3OCH3)=0.3mol·L-1,用H2表示反应②的速率是___________;可逆反应③的平衡常数K3=_____________。若在500K时,测得容器中n(CH3OH)=n(CH3OCH3),此时反应③v(正)_________v(逆),说明原因___________。
【答案】 -283.6 -24 K=c(H2O)×c(CH3OCH3)/[c2(CH4)×c(O2)] b bd 0.2 mol·L-1·min-1 2.25 > 因为体系中n(CH3OH)=n(CH3OCH3),有c(CH3OH)=c(CH3OCH3)= c(H2O),Qc=![]() =1<2.25,故反应正向程度大,v(正)>v(逆)
=1<2.25,故反应正向程度大,v(正)>v(逆)
【解析】(1)本题考查热化学反应方程式的计算,④甲烷的燃烧热:CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890.3kJ·mol-1,⑤二甲醚的燃烧热:CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(l) △H=-1453.kJ·mol-1,⑥H2O(l)=H2O(g) △H=+44.0kJ·mol-1,④×2-⑤+⑥得出:2CH4(g)+O2(g) ![]() CH3OCH3(g)+H2O(g) △H1=(-890.3×2+1453+44)kJ·mol-1=-283.6kJ·mol-1;△H3=反应物键能总和-生成物键能总和=2×(3×413+343+453)-(6×413+2×343+2×465)kJ·mol-1=-24kJ·mol-1;(2)考查化学平衡常数的表达,化学平衡状态的判断,根据化学平衡常数的定义,K=c(H2O)×c(CH3OCH3)/[c2(CH4)×c(O2)],反应①是放热反应,升高温度,平衡向逆反应方向移动,甲烷的体积分数增大,即曲线b正确;a、组分都是气体,气体的质量不变,条件是恒温恒容,容器的体积不变,因此密度不变,不能说明反应达到平衡,故错误;b、根据化学平衡状态的定义,当二甲醚的体积分数不变,说明反应达到平衡,故正确;c、没有反应速率进行的方向,因此不能确定反应达到平衡,故错误;d、条件是恒容状态,反应前后气体系数之和不相等,因此当压强不变时,说明反应达到平衡,故正确;(3)考查化学反应速率的计算和化学平衡常数的计算,CO(g)+2H2(g)
CH3OCH3(g)+H2O(g) △H1=(-890.3×2+1453+44)kJ·mol-1=-283.6kJ·mol-1;△H3=反应物键能总和-生成物键能总和=2×(3×413+343+453)-(6×413+2×343+2×465)kJ·mol-1=-24kJ·mol-1;(2)考查化学平衡常数的表达,化学平衡状态的判断,根据化学平衡常数的定义,K=c(H2O)×c(CH3OCH3)/[c2(CH4)×c(O2)],反应①是放热反应,升高温度,平衡向逆反应方向移动,甲烷的体积分数增大,即曲线b正确;a、组分都是气体,气体的质量不变,条件是恒温恒容,容器的体积不变,因此密度不变,不能说明反应达到平衡,故错误;b、根据化学平衡状态的定义,当二甲醚的体积分数不变,说明反应达到平衡,故正确;c、没有反应速率进行的方向,因此不能确定反应达到平衡,故错误;d、条件是恒容状态,反应前后气体系数之和不相等,因此当压强不变时,说明反应达到平衡,故正确;(3)考查化学反应速率的计算和化学平衡常数的计算,CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
起始(mol·L-1) 1 3 0
变化: 1×80% 1.6 0.8
平衡: 0.2 1.4 0.8
2CH3OH(g)![]() CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)
起始(mol·L-1) 0.8 0 0
变化: 2x x x
平衡: 0.8-2x x x 达到平衡时二甲醚的浓度为0.3mol·L-1,即x=0.3,根据化学反应速率的表达式,v(H2)=1.6/8mol/(L·min)=0.2 mol/(L·min),K=c(H2O)×c(CH3OCH3)/c2(CH3OH)=0.3×0.3/0.22=2.25,因为体系中n(CH3OH)=n(CH3OCH3),有c(CH3OH)=c(CH3OCH3)= c(H2O),Qc=![]() =1<2.25,故反应正向程度大,v(正)>v(逆)。
=1<2.25,故反应正向程度大,v(正)>v(逆)。

【题目】下列实验操作或事实与预期实验目的或所得结论一致的是
选项 | 实验操作或事实 | 实验目的或结论 |
A | 淡黄色试液 | 说明原溶液中一定含有FeCl3 |
B | Br2 | 制备少量KBr溶液 |
C | 无色试液 | 说明原溶液中一定不含钾元素 |
D | H3PO3+2NaOH(足量)=Na2HPO3+2H2O | H3PO3属于三元酸 |
A. A B. B C. C D. D