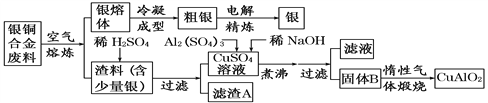
题目内容
【题目】向10.0mL0.10mol/L氨水中滴入0.10mol/L的盐酸,溶液的pH与所加盐酸的体积关系如图所示(假设无气体逸出),下列有关叙述正确的是

A. M~N间一定存在:c(Cl-)>c(NH4+)>c(OH-)>c(H+) B. M点对应的盐酸体积为10.0mL
C. M、N两点所示溶液中水的电离程度相同 D. P点处的溶液中存在2c(NH4+)+2c(NH3·H2O)=c(Cl-)
【答案】D
【解析】盐酸滴入氨水的过程中始终存在电荷守恒:c(NH4+)+c(H+)=c(OH-)+c(Cl-)。A项, 违背电荷守恒,错误;B项,若加入10.0mL盐酸,氨水与盐酸恰好完全反应获得NH4Cl溶液,NH4Cl溶液中由于NH4+的水解溶液呈酸性,M点pH=7,则M点对应盐酸体积小于10.0mL,错误;C项,N点为氨水,NH3·H2O电离出的OH-对水的电离起抑制作用,从N点到M点,随着盐酸的加入生成可水解的NH4Cl,水的电离程度逐渐增大,M点水的电离程度大于N点水的电离程度,错误;D项,P点加入20.0mL盐酸时,溶液中的物料守恒为2c(NH4+)+2c(NH3·H2O)=c(Cl-),正确;答案选D。

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目