题目内容
【题目】X,Y,Z是三种短周期的主族元素,在周期表的位置如图,X原子的最外层电子数是其次外层电子数的3倍,下列说法正确的是( ) 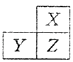
A.原子半径:Y>Z>X
B.气态氢化物的热稳定性:X<Z
C.y和z的最高价氧化物对应水化物均为强酸
D.若z的最高正价为+m,则X的最高正价也一定为+m
【答案】A
【解析】解:X、Y、Z是三种短周期的主族元素,由各元素在周期表中的位置可知,X处于第二周期,Y、Z处于第三周期.X原子的最外层电子数是其次外层电子数的3倍,则X最外层电子数为6,故X为氧元素,Z为硫元素,Y为磷元素.A、同周期随原子序数增大,原子半径减小,所以原子半Y>Z,同主族自上而下,原子半径增大,所以原子半径Z>X,故原子半径Y>Z>X,故A正确;
B、同主族自上而下,非金属性减弱,所以非金属性X>Z,非金属性越强,氢化物越稳定,所以气态氢化物的热稳定性X>Z,故B错误;
C、硫酸是强酸,磷酸属于中强酸,故C错误;
D、硫元素的最高正价为+6价,氧元素一般没有正化合价,故D错误.
故选:A.
X、Y、Z是三种短周期的主族元素,由各元素在周期表中的位置可知,X处于第二周期,Y、Z处于第三周期.X原子的最外层电子数是其次外层电子数的3倍,则X最外层电子数为6,故X为氧元素,Z为硫元素,Y为磷元素.结合元素周期律进行解答.

【题目】某化学学习小组的同学欲探究测定草酸晶体(H2C2O4xH2O)中x的值.通过查阅资料该小组同学得知:草酸易溶于水,其水溶液可以与酸性KMnO4溶液发生反应2MnO4﹣+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O.该组同学利用该反应原理设计了滴定的方法测定x值.
①称取1.260g纯草酸晶体,将其制成100.00mL水溶液为待测液.
②取25.00mL待测液放入锥形瓶中,再加入适量的稀H2SO4
③用浓度为0.1000mol/L的KMnO4标准溶液进行滴定,实验记录有关数据如下:
滴定次数 | 待测草酸溶液体积(mL) | 0.1000mol/LKMnO4标准溶液体积(mL) | |
滴定前刻度 | 滴定后刻度 | ||
第一次 | 25.00 | 0.00 | 10.02 |
第二次 | 25.00 | 0.22 | 11.32 |
第三次 | 25.00 | 1.56 | 11.54 |
请回答: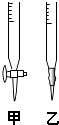
(1)滴定时,将KMnO4标准液装在右图中的(填“甲”或“乙”)滴定管中.
(2)本实验滴定达到终点的标志可以是 .
(3)通过上述数据,计算出x= .
(4)①若滴定终点时俯视滴定管刻度,则由此测得的x值会(填“偏大”、“偏小”或“不变”,下同).
②若滴定时所用的KMnO4溶液因久置而导致浓度变小,则由此测得的x值会 .