题目内容
(1)铅蓄电池的电池总反应式为:Pb+PbO2+4H++2SO42-
 2PbSO4+2H2O回答下列问题.(不考虑氢、氧的氧化还原)
2PbSO4+2H2O回答下列问题.(不考虑氢、氧的氧化还原)①放电时:负极的电极反应式是______,电解液中H2SO4的浓度将变______,当外电路通过2mol电子时,理论上负极板的质量增加______g.
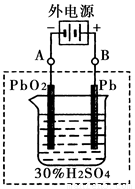
②在完全放电耗尽PbO2和Pb时,将原Pb和PbO2极板按右图连接,电解一段时间后,则在A电极上生成______,B电极上生成______.
(2)三氧化二镍(Ni2O3)可用于制造高能电池,其电解法制备过程如下:用NaOH调NiCl2溶液pH至7.5,加放适量硫酸钠后进行电解.电解过程中产生的Cl2在弱碱性条件下生成ClO-,把二价镍氧化为三价镍.以下说法正确的是______
a.可用铁作阳极材料
b.电解过程中阳极附近溶液的pH升高
c.阳极反应方程式为:2Cl--2e-=Cl2↑
d.1mol二价镍全部转化为三价镍时,外电路中通过了1mol电子.
【答案】分析:(1)由铅蓄电池的总反应PbO2+2H2SO4+Pb═2PbSO4+2H2O可知,放电时,Pb被氧化,应为电池负极反应,电极反应式为Pb-2e-+SO42-=PbSO4,正极上PbO2得电子被还原,电极反应式为PbO2+SO42-+2e-+4H+═PbSO4+2H2O,在充电时,阳极上发生氧化反应,阴极上发生还原反应;
(2)阳极发生氧化反应生成氯气,应用惰性电极,发生2Cl--2e-=Cl2↑,Cl2在弱碱性条件下生成ClO-,把二价镍氧化为三价镍.
解答:解:(1)①Pb+PbO2+4H++2SO42-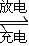 2PbSO4+2H2O,该反应中Pb作为负极,所以负极的电极反应式是Pb+SO42--2e-=PbSO4,反应过程中消耗了硫酸,所以电解液中H2SO4的浓度将变小;该反应转移的电子数为2,所以当外电路通过2mol电子时,即有1mol的Pb发生反应,所以在负极增加一摩尔硫酸根的质量,即负极板的质量增加96g,故答案为:Pb+SO42--2e-=PbSO4;小;96;
2PbSO4+2H2O,该反应中Pb作为负极,所以负极的电极反应式是Pb+SO42--2e-=PbSO4,反应过程中消耗了硫酸,所以电解液中H2SO4的浓度将变小;该反应转移的电子数为2,所以当外电路通过2mol电子时,即有1mol的Pb发生反应,所以在负极增加一摩尔硫酸根的质量,即负极板的质量增加96g,故答案为:Pb+SO42--2e-=PbSO4;小;96;
②该过程为放电的逆过程,所以在A电极上生成Pb,在B电极上生成PbO2,故答案为:Pb; PbO2;
(2)阳极发生的是氧化反应,所以不能用铁作阳极材料,故a错误;
阳极反应方程式为:2Cl--2e-=Cl2↑,Cl2在弱碱性条件下生成ClO-,故电解过程中阳极附近溶液的pH降低,故b错误,c正确,1 mol二价镍全部转化为三价镍时,外电路中通过了1mol电子,故d正确,
故答案为:cd.
点评:本题考查了原电池、电解池的知识,该考点是高考考查的重点和难点,本题有一定的综合性,难度适中.
(2)阳极发生氧化反应生成氯气,应用惰性电极,发生2Cl--2e-=Cl2↑,Cl2在弱碱性条件下生成ClO-,把二价镍氧化为三价镍.
解答:解:(1)①Pb+PbO2+4H++2SO42-
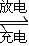 2PbSO4+2H2O,该反应中Pb作为负极,所以负极的电极反应式是Pb+SO42--2e-=PbSO4,反应过程中消耗了硫酸,所以电解液中H2SO4的浓度将变小;该反应转移的电子数为2,所以当外电路通过2mol电子时,即有1mol的Pb发生反应,所以在负极增加一摩尔硫酸根的质量,即负极板的质量增加96g,故答案为:Pb+SO42--2e-=PbSO4;小;96;
2PbSO4+2H2O,该反应中Pb作为负极,所以负极的电极反应式是Pb+SO42--2e-=PbSO4,反应过程中消耗了硫酸,所以电解液中H2SO4的浓度将变小;该反应转移的电子数为2,所以当外电路通过2mol电子时,即有1mol的Pb发生反应,所以在负极增加一摩尔硫酸根的质量,即负极板的质量增加96g,故答案为:Pb+SO42--2e-=PbSO4;小;96;②该过程为放电的逆过程,所以在A电极上生成Pb,在B电极上生成PbO2,故答案为:Pb; PbO2;
(2)阳极发生的是氧化反应,所以不能用铁作阳极材料,故a错误;
阳极反应方程式为:2Cl--2e-=Cl2↑,Cl2在弱碱性条件下生成ClO-,故电解过程中阳极附近溶液的pH降低,故b错误,c正确,1 mol二价镍全部转化为三价镍时,外电路中通过了1mol电子,故d正确,
故答案为:cd.
点评:本题考查了原电池、电解池的知识,该考点是高考考查的重点和难点,本题有一定的综合性,难度适中.

练习册系列答案
相关题目
(1)铅蓄电池的电池总反应式为:
Pb+PbO2+4H++2SO42- ![]() 2PbSO4+2H2O回答下列
2PbSO4+2H2O回答下列
 |
问题。(不考虑氢、氧的氧化还原)
①放电时:负极的电极反应式是 ,
电解液中H2SO4的浓度将变________,当外电路通过
2mol电子时,理论上负极板的质量增加 g。
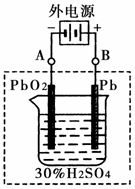
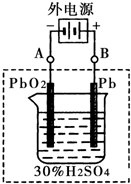
②在完全放电耗尽PbO2和Pb时,将原Pb和PbO2极板
按右图连接,电解一段时间后,则在A电极上生成 __________,B电极上?生成________。
(2)三氧化二镍(Ni2O3)可用于制造高能电池,其电解法制备过程如下:用NaOH调NiCl2溶液pH至7.5,加放适量硫酸钠后进行电解。电解过程中产生的Cl2在弱碱性条件下生成ClO-,把二价镍氧化为三价镍。以下说法正确的是
a.可用铁作阳极材料
b.电解过程中阳极附近溶液的pH升高
c.阳极反应方程式为:2Cl--2e-=Cl2↑
d.1 mol二价镍全部转化为三价镍时,外电路中通过了1mol电子。
 (1)铅蓄电池的电池总反应式为:
(1)铅蓄电池的电池总反应式为: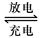 2PbSO4+2H2O回答下列 问题。(不考虑氢、氧的氧化还原)
2PbSO4+2H2O回答下列 问题。(不考虑氢、氧的氧化还原)
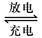 2PbSO4+2H2O回答下列
问题。(不考虑氢、氧的氧化还原)
2PbSO4+2H2O回答下列
问题。(不考虑氢、氧的氧化还原)