题目内容
【题目】向盛有一定量烧碱溶液的烧杯中通入一定量的CO2 气体后,再向所得溶液中逐滴加入盐酸至过量,产生的 CO2 气体与加入 HCl 的物质的量的关系如下图所示(忽略 CO2 的溶解和 HCl的挥发):
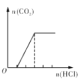
请问图中O点对应溶液的溶质为_____(填化学式),其物质的量之比为_____。开始产生 CO2 气体时对应的离子方程式为_____。
【答案】Na2CO3、NaHCO3 1:1 HCO3- + H+ =CO2↑+H2O
【解析】
Na2CO3跟盐酸的反应是分步进行的:Na2CO3+HCl=NaHCO3+NaCl,NaHCO3+HCl=NaCl+H2O+CO2↑,由图象可知生成二氧化碳消耗的HCl的物质的量大于从反应到开始产生二氧化碳阶段消耗的HCl,则氢氧化钠与二氧化碳反应后的溶质为NaHCO3、Na2CO3,由此分析解答;
Na2CO3跟盐酸的反应是分步进行的:Na2CO3+HCl=NaHCO3+NaCl,NaHCO3+HCl=NaCl+H2O+CO2↑,由图象可知生成二氧化碳消耗的HCl的物质的量大于从反应到开始产生二氧化碳阶段消耗的HCl,则氢氧化钠与二氧化碳反应后的溶质为NaHCO3、Na2CO3。由图可知,从O点到开始产生气体与开始产生气体到产生气体消耗盐酸最大量的体积之比为1:2,所以NaHCO3和Na2CO3的物质的量之比为1:1,开始产生 CO2 气体时对应的离子方程式为:HCO3- + H+ =CO2↑+H2O故答案为:NaHCO3、Na2CO3;1:1;HCO3- + H+ =CO2↑+H2O

练习册系列答案
相关题目