题目内容
(10分)
2006年世界锂离子电池总产量超过25亿只,锂电池消耗量巨大,对不可再生的金属资源的消耗是相当大的。因此锂离子电池回收具有重要意义,其中需要重点回收的是正极材料,其主要成分为钴酸锂(LiCoO2)、导电乙炔黑(一种炭黑)、铝箔以及有机粘接剂。某回收工艺流程如下:
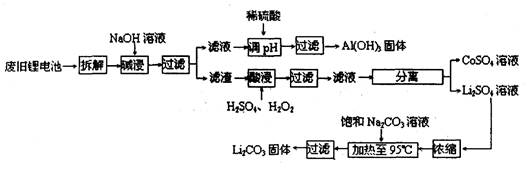
(1)上述工艺回收到的产物有
(2)Li原子的最外层电子数是 ,废旧电池可能由于放电不完全而残留有原子态的锂,为了安全对拆解环境的要求是___________________________________________
(3)碱浸时主要反应的化学方程式为 。
(4)最后一步过滤应趁热过滤,原因是
2006年世界锂离子电池总产量超过25亿只,锂电池消耗量巨大,对不可再生的金属资源的消耗是相当大的。因此锂离子电池回收具有重要意义,其中需要重点回收的是正极材料,其主要成分为钴酸锂(LiCoO2)、导电乙炔黑(一种炭黑)、铝箔以及有机粘接剂。某回收工艺流程如下:

(1)上述工艺回收到的产物有
(2)Li原子的最外层电子数是 ,废旧电池可能由于放电不完全而残留有原子态的锂,为了安全对拆解环境的要求是___________________________________________
(3)碱浸时主要反应的化学方程式为 。
(4)最后一步过滤应趁热过滤,原因是
(1)LiCoO2、Al(OH)3、CoSO4
(2)1,隔绝空气和水
(3)2Al + 2NaOH + 2H2O = 2NaAlO2 + 3H2↑
(4)防止析出硫酸钠晶体。
(2)1,隔绝空气和水
(3)2Al + 2NaOH + 2H2O = 2NaAlO2 + 3H2↑
(4)防止析出硫酸钠晶体。
(1)根据流程图可知,回收到的产物有Al(OH)3、CoSO4和Li2CO3。(2)Li是3号元素,最外层一个电子。锂与钠为同一主族,易与水和氧气反应,所以要隔绝空气和水(3)碱浸时,只有铝箔能跟NaOH反应。Na2CO3与LiSO4反应生成Li2CO3沉淀和Na2SO4溶液,Na2SO4溶液冷却会析出固体,所以要趁热过滤。

练习册系列答案
 综合自测系列答案
综合自测系列答案
相关题目
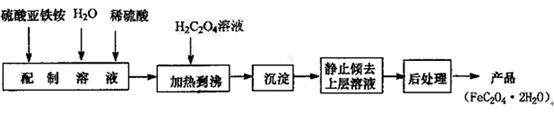
 6H2O溶液时,需加少量稀硫酸,目的是 。
6H2O溶液时,需加少量稀硫酸,目的是 。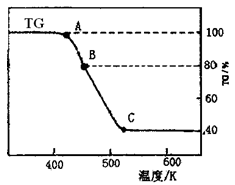
 Fe(s)+CO2(g)反应平衡常数K=0.4,则该反应达平衡时,FeO的转化率为多少? 。
Fe(s)+CO2(g)反应平衡常数K=0.4,则该反应达平衡时,FeO的转化率为多少? 。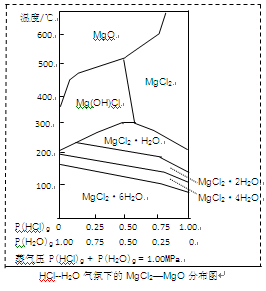
 ,降低机动车辆尾气中有害气体排放
,降低机动车辆尾气中有害气体排放